Oralni Lihen Planus i Oralne Lihenoidne Lezije
Oralni lihen planus (OLP) i oralne lihenoidne lezije (OLL) su skupina poremećaja oralne sluznice koji vjerojatno predstavljaju obrazac uobičajenih reakcija kao odgovor na ekstrinzične antigene, promijenjene autoantigene i superantigene.
Povijesno gledano, vezano za terminologiju OLP i OLL, nakon brojnih nerazriješenih rasprava i kontroverzi, još uvijek nedostaju definitivni klinički dijagnostički i histološki kriteriji za razlikovanje OLP-a od OLL-a. Također ne postoji konsenzus o mogućim kliničkim i bihevioralnim razlikama u pogledu rizika zloćudne transformacije između OLP-a i OLL-a.
Prema klasifikaciji iz 2005. godine OLP je uvršten kao potencijalno zloćudni poremećaj, što je potvrđeno i na nedavnoj radionici Svjetske zdravstvene organizacije – “Collaborating Center for oral Cancer Workshop ” – održanoj u Ujedinjenom Kraljevstvu 2020. godine.
Oralni Lihen Planus
OLP se definiran kao „kronični upalni poremećaj nepoznate etiologije s karakterističnim relapsima i remisijama, a koji se pojavljuje u obliku bijelih retikularnih lezija, koje mogu biti praćene atrofičnim, erozivnim i ulcerativnim i/ili plakoznim područjima.” Lezije su često bilateralno simetrične. Može biti prisutan i deskvamativni gingivitis.
Prevalencija:
- Procijenjena prevalencija u populaciji kreće se od 1-3%. OLP je najčešća mukokutana bolest usne šupljine.
- Preferencija prema ženskom spolu
- Povećan rizik od nastanka OLP-a je nakon 40 -te godine starosti, s prosječnom dobi pojavljivanja od 50-55 godina.
Zloćudna Preobrazba:
U analizi koja je uključivala isključivo visoko kvalitetne publikacije, autori su zabilježilistopu zloćudne preobrazbe od 2.28% za OLP.
Rizični Čimbenici:
- lokalizacija na jeziku
- prisutnost atrofičnih/erozivnih lezija
- konzumacija duhana i alkohola
- humani papiloma virus
- hepatitis C virus (HCV)
- prisutnost aneuploidije
Najveći rizik za razvoj oralnog karcinoma je između 3. i 6. godine od prve dijagnoze OLP-a.
Bolesnici s OLP i OLL mogu razviti višestruke zloćudne lezije, koje ne nastaju uvijek na mjestu već postojećih lezija. Oralni planocelularni karcinom koji se razvija u bolesnika s OLP i OLL pokazuje povoljne prognostičke parametre, posebice u pogledu stope mortaliteta.
Klinička Slika:
Prepoznatljive kliničke karakteristike OLP-a podrazumijevaju prisutnost bijelih papula koje se povećavaju i spajaju formirajući retikularni, prstenasti ili uzorak nalik plaku, takozvane Wickhamove strije.
- Opisano je 6 kliničkih podtipova OLP-a, koji se mogu pojaviti pojedinačno ili u kombinaciji: retikularni, plakozni, atrofični, erozivni/ulcerozni, papularni i bulozni. Raspravljamo o 2 podtipa (keratotični/bijeli i eritematozni/crveni).
- Obično je istovremeno prisutno više podtipova.
- Najčešće zahvaćena područja su obrazna sluznica, dorzum i lateralne strane jezika te gingiva.
- Gotovo uvijek je prisutna manje više simetrična bilateralna distribucija
- Tijek bolesti karakteriziraju periodi recidivia i remisije, s razmacima od nekoliko tjedana ili mjeseci te kliničkim znakovima i simptomima.
Keratotični/Bijeli Oralni Lihen Planus:
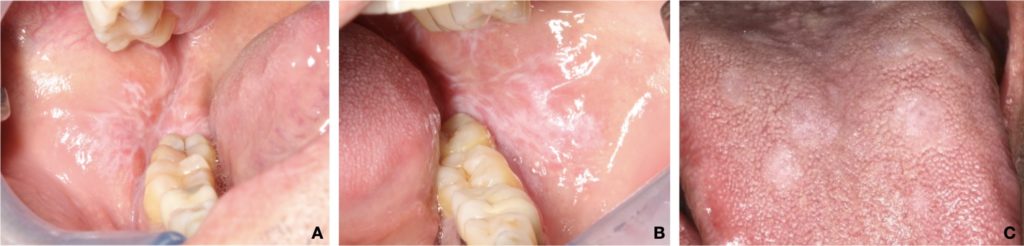
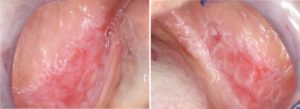
- Najčešći oblik OLP-a, karakteriziran je pojavom simetričnih bijelih retikularnih lezija (Wickhamove strije), a rjeđe bijelih papula ili plakova (Slika 1.).
- Plakozni oblik OLP-a izgleda kao homogeni, blago povišeni, multifokalni bijeli plak, koji tipično zahvaća jezik i obraznu sluznicu (Slika 2c).
- Općenito asimptomatski – obično slučajan nalaz tijekom rutinskog pregleda usne šupljine od strane stomatologa.
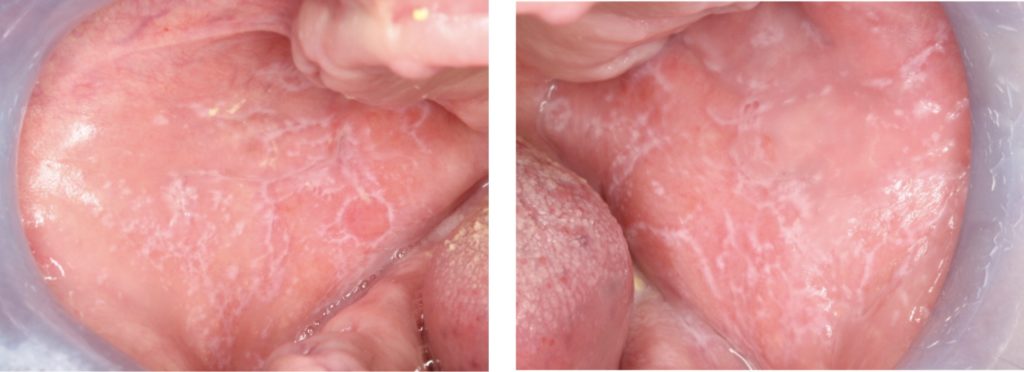
Eritematozni/Crveni Oralni Lihen Planus:
- Može se pojaviti kao područje atrofične sluznice ili kao crvene lezije zbog hiperemije oralne sluznice.
- Područja eritema mogu biti popraćena ulceracijom i često uz prisutnost bijelih keratotičnih strija (Slika 4.).
- Simptomi variraju od blagog osjećaja peckanja do jake boli. Lezije mogu otežavati govor, žvakanje i gutanje.
Deskvamativni Gingivitis:
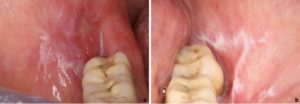
- Erozivni lihen planus lokaliziran na gingivi u obliku deskvamativnog gingivitisa (Slika 6.)
- OLP je najčešći uzrok deskvamativnog gingivitisa nakon pemfigoida i pemfigusa (23).
- Najčešće je zahvaćena gingiva s bukalne strane.
Ekstraoralne Manifestacije:
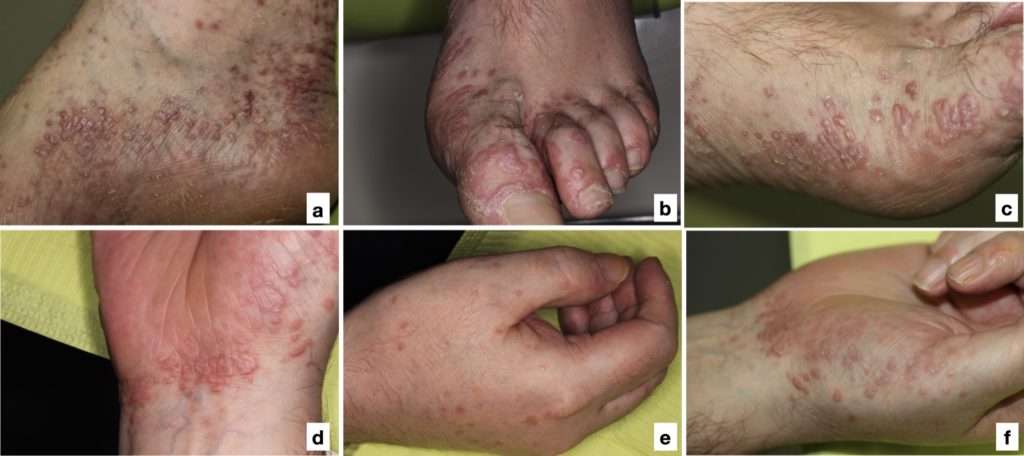
- 15% bolesnika s OLP-om razvije kožni lihen planus, do 60% bolesnika s kožnim lihenom planusom ima oralne manifestacije
- Pojavljuje se kao papuloskvamozni osip s ljubičastim izbočinama ravnog vrha, različite veličine, koji se često opisuje kao “6 Ps” (ljubičasti, svrbež, poligonalni, ravni, papule i plakovi), karakteriziran klasičnim Wickhamovim strijama
- Tipično je lokaliziran na ekstremitetima (slika 7), ali povremeno može biti generaliziran i zahvaćati vlasište i nokte.
- Ostale anatomske lokalizacije koje mogu biti zahvaćene uključuju genitalnu sluznicu, te sluznicu jednjaka, oka, mokraćnog sustava, nosa, grkljana, uha, želuca i analne regije.
Povezanost sa sistemskim bolestima:
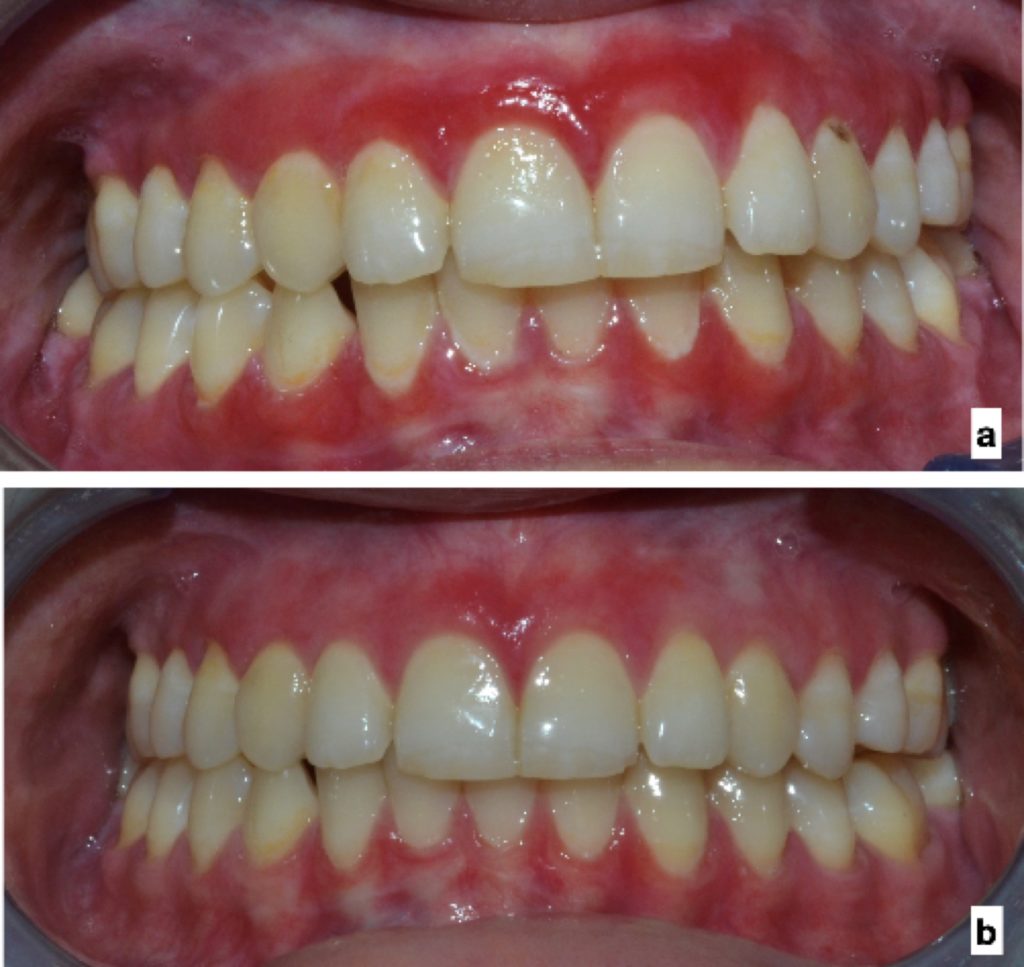
OLP se povezuje s različitim sistemskim bolestima, uključujući hepatitis C, hipertenziju, dijabetes i bolesti štitnjače
Postoje čvrsti dokazi o povezanosti HCV s OLP-om te o njegovoj vjerojatnoj uključenosti u patogenezu. Čini se kako bi bilo razborito od bolesnika s OLP-om dobiti informaciju o čimbenicima rizika povezanim s HCV-om te zatražiti određivanje HCV antitijela ukoliko je opravdano.
Diferencijalna Dijagnoza:
- Retikularne i eritematozne lezije: OLL i diskoidni eritemsku lupus
- Atrofični i ulcerozni oblici: pemphigus vulgaris, pemfigoid i linearna IgA bolest (diferencira se po prisutnosti retikularne mrežice).
- Plakozni oblik: oralna leukoplakia, proliferativna verukozna leukoplakija (PVL)
Bez obzira na početnu dijagnozu, bolesnike s bijelim multifokalnim lezijama treba pažljivo pratiti zbog rane detekcije zloćudne preobrazbe.
Dijagnoza:
- Uključuje procjenu kliničke slike
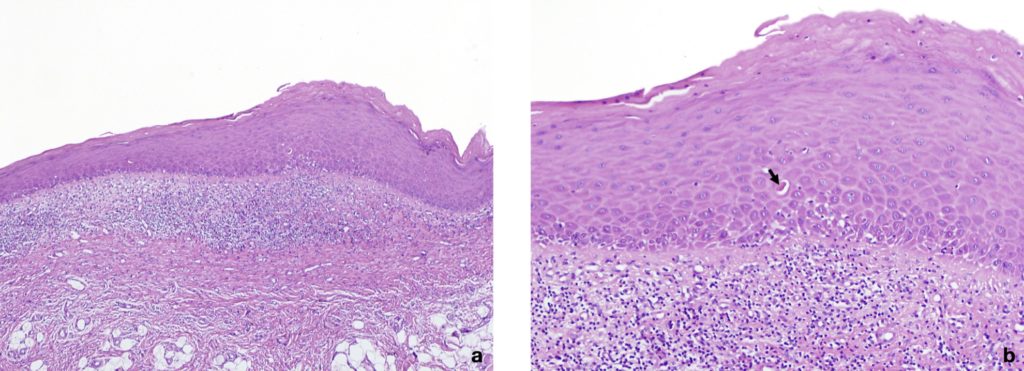
- Za potvrdu dijagnoze potrebno je napraviti biopsiju i patohistološki nalaz zbog potrebe dugotrajnog liječenja i rizika od zloćudne preobrazbe
| Tip | Nalazi |
| Klinički kriteriji | Prisutnost bilateralnih, manje ili više simetričnih bijelih lezija koje zahvaćaju obraznu sluznicu, jezik, usne i/ili gingivu. Prisutnost bijelih papuloznih lezija i čipkaste mreže blago podignutih bijelih linija (retikularni, prstenasti ili linearni uzorak) sa ili bez erozija i ulceracija. Ponekad se manifestira kao deskvamativni gingivitis. |
| Histopatološki kriteriji | Prisutnost dobro definiranog vrpčastog, pretežno limfocitnog infiltrata koji je ograničen na površinski dio vezivnog tkiva. Znakovi vakuolarne degeneracije bazalnih i/ili suprabazalnih slojeva stanica s apoptozom keratinocita. Kod atrofičnog tipa dolazi do stanjivanja epitela, a ponekad i do ulceracija uzrokovanih neuspjehom regeneracije epitela kao posljedica razaranja bazalnih stanica. Može biti prisutan i mješoviti upalni infiltrat. |
Table 1: Dijagnostički kriterij za Oralni lihen planus (Prilagođeno prema Warnakulasuriya i sur., 2020)
Liječenje:
- Glavni cilj liječenja OLP je ublažavanje simptoma – bolesnici s retikularnim lezijama i drugim asimptomatskim lezijama ne trebaju liječenje
- Najprije treba identificirati i isključiti okidače i otežavajuće čimbenike (oštri ili slomljeni zubi, loše postavljena proteza itd.).
- Bolesnike treba savjetovati da prestanu s konzumiranjem duhana i alkohola jer isti mogu povećati rizik od zloćudne transformacije. Bolesnike također treba poučiti da održavaju dobru oralnu higijenu, jer smanjenje zubnih naslaga može imati povoljan učinak na gingivne lezije.
- Natrij-lauril sulfat (SLS) je sredstvo za stvaranje pjene koje se dodaje zubnim pastama a može pogoršati simptome, te se stoga preporuča korištenje paste za zube bez SLS-a.
- Olakšanje simptoma može se postići upotrebom lokalnih anestetika kao što je 0,15% benzidamin hidroklorid (kao sprej ili tekućina za ispiranje usta) ili lidokain gel.
- Prva linija terapije za OLP su topikalni kortikosteroidi. Dostupan je niz pripravaka koji se mogu koristiti kao vodice za ispiranje usta: tablete betametazon natrijevog fosfata od 500 mikrograma otopljene u 10 ml vode do četiri puta dnevno, tablete prednizolona od 5 mg otopljene u 10 ml vode ili fliksonaze ampule od 400 mikrograma u 10 ml vode dva puta dnevno. Flutikazon propionat sprej (50 mikrograma/udah) usmjeren na zahvaćena područja 3-4 puta dnevno koristan je za izolirane lezije.
- Za deskvamativni gingivitis koriste se preparati s kortikosteroidima u obliku gela koji se nanose u individualno prilagođene udlage, izrađene od meke prozirne smole ili silikona kako bi se produžilo vrijeme kontakta.
Praćenje
- Zbog rizika zloćudne preobrazbe, redovito praćenje je potrebno kako bi se detektirao relaps bolesti.
- Učestalost kontrolnih pregleda povećava se proporcionalno s aktivnošću i simptomima bolesti.
- Preporuka je minimalno jedan kontrolni pregled godišnje a po mogućnosti i 2 do 4 godišnja pregleda ovisno o znakovima i simptomima OLP-a.
- Ukoliko se tijekom kontrolnih pregleda uoče nove promjene na leziji, potrebno je napraviti biopsiju i skratiti intervale praćenja.
Oralne Lihenoidne Lezije
Lihenoidne lezije su crvene/bijele intraoralne lezije s retikularnim strijama izgledom slične OLP-u, ali se povezuju s različitim poznatim čimbenicima. Lezije se mogu podijeliti na oralne lihenoidne kontaktne lezije, lijekovima izazvane OLL i GVHD-inducirane OLL.
Oralne Lihenoidne Kontaktne Lezijes:
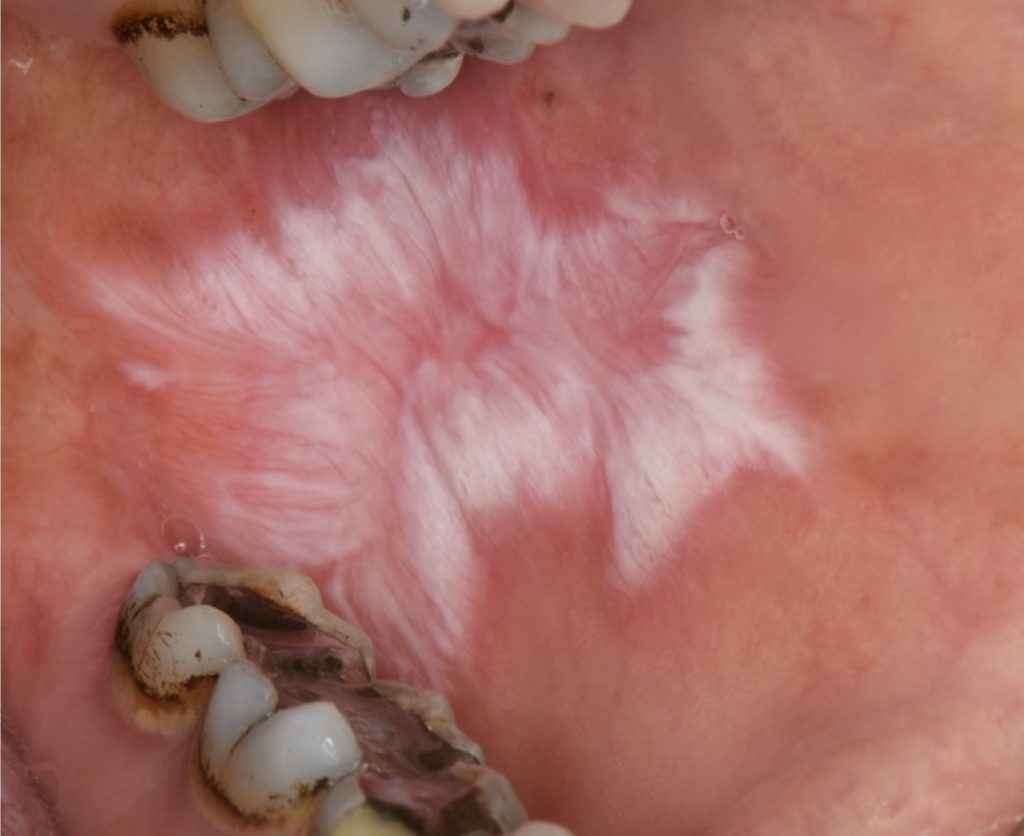
- Oralne lihenoidne kontaktne lezije koriste se za opisivanje oralnih lezija koje klinički i histopatološki podsjećaju na lihen planus.
- Smatra se da je uzrokovana lokalnom reakcijom preosjetljivosti (preosjetljivost posredovana odgođenim imunitetom) na dentalni restaurativni materijal (amalgam, zlato, nikal, akrilna smola) ili druga sredstva (npr. cimet).
- Pojavljuju se kao bijele lezije ili mješovite crveno-bijele lezije, povremeno ulcerirane. Oralne lihenoidne kontaktne lezije su općenito manje simetrične i češće jednostrane od OLP-a te im može nedostajati tipični retikularni izgled OLP-a, češće se pojavljuju kao plakozni ili atrofični oblik.
- Dijagnostička karakteristika je topografsko mjesto u izravnom kontaktu s suspektnim uzročnikom.
» Show more
- Čini se kako je trajanje kontakta između uzročnika i oralne sluznice važan čimbenik u razvoju Oralnih lihenoidnih kontaktnih lezija
- Dijagnoza se obično temelji na kliničkim nalazima, a nestanak lezije nakon eliminacije/zamjene restaurativnog materijala ili mogućeg uzročnika potvrđuje dijagnozu.
- Može se napraviti test zakrpe (“patch test”) kako bi se identificirala potencijalna reakcija preosjetljivosti; međutim, studije o njegovoj koristi za dijagnosticiranje oralnih kontaktnih lihenoidnih lezija pokazale su oprečne rezultate. Provođenje testa također može biti od pomoći prilikom odabira alternativnog restaurativnog materijala.
- Kliničari bi s bolesnicima trebali raspraviti o potencijalnim prednostima i rizicima uklanjanja amalgamskih ispuna, spomenuti periodičku prirodu bolesti, koju karakteriziraju razdoblja pogoršanja i spontane remisije, te nepredvidljivost postupka uklanjanja amalgama u povlačenju lezija.
» View less
Lijekovima izazvane oralne lihenoidne lezije
- Uzrokovane ili povezane s izloženošću određenim lijekovima, rijetke su za razliku od kožnih OLL
- Duga je lista sistemskih lijekova koji se povezuju s pojavom OLL-a, a uključuje nesteroidne protuupalne lijekove, antihipertenzive, oralne hipoglikemike, antibiotike, antifungalne lijekove i monoklonska antitijela
- Obično vremenska povezanost između pojave oralnih i/ili kožnih lezija i uzimanja određenih lijekova; međutim, reakcija na lijek se može pojaviti u bilo kojem trenutku, uključujući i godine nakon njegovog uvođenja
» Show more
- Klinički izgled je nejasan, posebno u usporedbi s drugim lihenoidnim lezijama, iako jednostrano pojava promjena može pomoći u postavljanju dijagnoze
- Dijagnoza se potvrđuje kada nastupi regresije lezije nakon ukidanja ili promjene mogućeg uzročnog lijeka te nakon ponovne pojave lezije uslijed ponovnog početka liječenja istim lijekom
- Lijekove treba ukinuti tek nakon savjetovanja s bolesnikovim liječnikom, a ova praksa nije uvijek izvediva u bolesnika koji uzimaju više lijekova
» View less
Bolest presatka protiv primatelja (GVHD)
- GVHD je komplikacija koja se javlja u primatelja nakon transplantacije krvotvornih matičnih stanica.
- Sistemsko stanje s različitim znakovima i simptomima, zahvaća više organa, uključujući kožu, usnu šupljinu, oči, gastrointestinalni trakt i jetru, kao i druge sustave poput pluća, zglobova i genitourinarnog trakta.
- Oralne promjene kod akutnog GVHD-a su iznimno rijetke, međutim, usna šupljina jedno je od najčešće zahvaćenih mjesta kod kroničnog GVHD-a.
- Oralne promjene kod kroničnog GVHD-a klinički karakterizira pojava lihenoidne upale koja često zahvaća jezik i oralnu sluznicu, ali može zahvatiti bilo koje mjesto u usnoj šupljini i može varirati od ograničene bolesti sa samo blagim promjenama do opsežnije i simptomatske bolest.
- Kliničke promjene uključuju papule, bijele plakove i hiperkeratotične strije koje podsjećaju na Wickhamove strije kod OLP, kao i eritem te ulceracije prekrivene pseudomembranama.
- Kliničke karakteristike često su dovoljne za postavljanje dijagnoze, pod uvjetom da su prisutne u kontekstu bolesnika koji je podvrgnut alogenskoj transplantaciji krvotvornih matičnih stanica
Literatura
Khudhur AS, Di Zenzo G, Carrozzo M. Oral lichenoid tissue reactions: diagnosis and classification. Expert Rev Mol Diagn. 2014;14:169‐184.
Carrozzo M, Porter S, Mercadante V, Fedele S. Oral lichen planus: A disease or a spectrum of tissue reactions? Types, causes, diagnostic algorhythms, prognosis, management strategies. Periodontol 2000. 2019 Jun;80(1):105-125.
Warnakulasuriya S, Kujan O, Aguirre-Urizar JM, Bagan JV, González-Moles MÁ, Kerr AR, et al. Oral potentially malignant disorders: A consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2020 (In press)
McCartan BE, Healy CM. The reported prevalence of oral lichen planus: a review and critique. J Oral Pathol Med 2008;37(8):447–53.
González-Moles MA, Warnakulasuriya S, González-Ruiz I, González-Ruiz L, Ayén Á, Lenouvel D, Ruiz-Ávila I, Ramos-García P. Worldwide prevalence of oral lichen planus: A systematic review and meta-analysis. Oral Dis 2020 (In press)
Warnakulasuriya S. White, red, and mixed lesions of oral mucosa: A clinicopathologic approach to diagnosis. Periodontol 2000 2019;80(1):89-104.
van der Meij EH, Mast H, van der Waal I. The possible premalignant character of oral lichen planus and oral lichenoid lesions: a prospective five-year follow-up study of 192 patients. Oral Oncol. 2007;43(8):742-8
Fitzpatrick SG, Hirsch SA, Gordon SC. The malignant transformation of oral lichen planus and oral lichenoid lesions: a systematic review. J Am Dent Assoc. 2014 Jan;145(1):45-56.
Aghbari SMH, Abushouk AI, Attia A, Elmaraezy A, Menshawy A, Ahmed MS, Elsaadany BA, Ahmed EM. Malignant transformation of oral lichen planus and oral lichenoid lesions: A meta-analysis of 20095 patient data. Oral Oncol. 2017;68:92-102
González-Moles MÁ, Ruiz-Ávila I, González-Ruiz L, Ayén Á, Gil-Montoya JA, Ramos-García P. Malignant transformation risk of oral lichen planus: A systematic review and comprehensive meta-analysis. Oral Oncol. 2019;96:121-130
González-Moles MÁ, Warnakulasuriya S, González-Ruiz I, González-Ruiz L, Ayén Á, Lenouvel D, et al. Clinical interpretation of findings from a systematic review and a comprehensive meta-analysis on clinicopathological and prognostic characteristics of oral squamous cell carcinomas (OSCC) arising in patients with oral lichen planus (OLP): Author’s reply. Oral Oncol. 2020 (In press).
González-Moles MÁ, Ramos-García P, Warnakulasuriya S. An appraisal of highest quality studies reporting malignant transformation of oral lichen planus based on a systematic review. Oral Dis. 2020 (In press).
Idrees M, Kujan O, Shearston K, Farah CS. Oral lichen planus has a very low malignant transformation rate: A systematic review and meta-analysis using strict diagnostic and inclusion criteria. J Oral Pathol Med. 2020 (in Press).
Speight PM, Khurram SA, Kujan O. Oral potentially malignant disorders: risk of progression to malignancy. Oral Surg Oral Med Oral Pathol Oral Radiol. 2018;125(6):612-627.
Gonzalez-Moles MA, Scully C, Gil-Montoya JA. Oral lichen planus: controversies surrounding malignant transformation. Oral Dis 2008; 14:229–243.
Mignogna MD, Fedele S, Lo Russo L, Mignogna C, de Rosa G, Porter SR. Field cancerization in oral lichen planus. Eur J Surg Oncol. 2007;33(3):383-9
González-Moles MÁ, Warnakulasuriya S, González-Ruiz I, González-Ruiz L, Ayén Á, Lenouvel D, Ruiz-Ávila I, Ramos-García P. Clinicopathological and prognostic characteristics of oral squamous cell carcinomas arising in patients with oral lichen planus: A systematic review and a comprehensive meta-analysis. Oral Oncol. 2020 (In press)
Andreasen JO. Oral lichen planus. 1. A clinical evaluation of 115 cases. Oral Surg Oral Med Oral Pathol 1968;25(1):31–42.
Alrashdan MS, Cirillo N, McCullough M. Oral lichen planus: a literature review and update. Arch Dermatol Res. 2016;308(8):539-51.
Silverman S Jr, Gorsky M, Lozada-Nur F. A prospective follow-up study of 570 patients with oral lichen planus: persistence, remission, and malignant association. Oral Surg Oral Med Oral Pathol. 1985;60(1):30-4
Au J, Patel D, Campbell JH. Oral lichen planus. Oral Maxillofac Surg Clin North Am. 2013 Feb;25(1):93-100, vii.
De Rossi SS, Ciarrocca K. Oral lichen planus and lichenoid mucositis. Dent Clin North Am 2014;58: 299–313.
Leao JC, Ingafou M, Khan A, Scully C, Porter S. Desquamative gingivitis: retrospective analysis of disease associations of a large cohort. Oral Dis. 2008;14(6):556–60.
Müller S. Oral lichenoid lesions: distinguishing the benign from the deadly. Mod Pathol. 2017 Jan;30(s1):S54-S67.
Scully C, Carrozzo M Oral mucosal disease: lichen planus. Br J Oral Maxillofac Surg 2008; 46:15–21.
Robledo-Sierra J, van der Waal I. How general dentists could manage a patient with oral lichen planus. Med Oral Patol Oral Cir Bucal. 2018;23(2):e198-e202
Tziotzios C, Lee JYW, Brier T, Saito R, Hsu CK, Bhargava K, Stefanato CM, Fenton DA, McGrath JA. Lichen planus and lichenoid dermatoses: Clinical overview and molecular basis. J Am Acad Dermatol. 2018;79(5):789-804.
Parashar P. Oral lichen planus. Otolaryngol Clin North Am 2011;44:89–107.
Fox LP, Lightdale CJ, Grossman ME. Lichen planus of the esophagus: what dermatologists need to know. J Am Acad Dermatol. 2011;65(1):175-83
Eisen D. The evaluation of cutaneous, genital, scalp, nail, esophageal,and ocular involvement in patients with oral lichen planus.Oral SurgOral Med Oral Pathol Oral Radiol Endod 1999;88:431–6
Cassol-Spanemberg J, Rodríguez-de Rivera-Campillo ME, Otero-Rey EM, Estrugo-Devesa A, Jané-Salas E, López-López J. Oral lichen planus and its relationship with systemic diseases. A review of evidence. J Clin Exp Dent. 2018;10(9):e938-e944.
Baccaglini L, Thongprasom K, Carrozzo M, Bigby M. Urban legends series: lichen planus. Oral Dis. 2013;19(2):128-43
Bigby M. The relationship between lichen planus and hepatitis C clarified. Arch Dermatol 2009; 145: 1048–1050.
Kuten-Shorrer M, Menon RS, Lerman MA. Mucocutaneous Diseases. Dent Clin North Am. 2020 Jan;64(1):139-162.
Lopes MA, Feio P, Santos-Silva AR, Vargas PA. Proliferative verrucous leukoplakia may initially mimic lichenoid reactions. World J Clin Cases. 2015 Oct 16;3(10):861-3
McParland H, Warnakulasuriya S. Lichenoid morphology could be an early feature of oral proliferative verrucous leukoplakia. J Oral Pathol Med. 2020 (In press)
Gilligan G, Garola F, Piemonte E, Leonardi N, Panico R, Warnakulasuriya S. Lichenoid proliferative leukoplakia, lichenoid lesions with evolution to proliferative leukoplakia or a continuum of the same precancerous condition? A revised hypothesis. J Oral Pathol Med. 2020 (In press)
Van der Meij EH, Van der Waal I. Lack of clinicopathologic correlation in the diagnosis of oral lichen planus based on the presently available diagnostic criteria and suggestions for modifications. J Oral Pathol Med. 2003;32:507‐512.
Eisenberg E. Clinical controversies in oral and maxillofacial surgery: part one. Oral lichen planus: a benign lesion. J Oral Maxillofac Surg 2000;58:1278-85.
Al-Hashimi I, Schifter M, Lockhart PB, Wray D, Brennan M, Migliorati CA, et al. Oral lichen planus and oral lichenoid lesions: diagnostic and therapeutic considerations. Oral Surg Oral Med Oral Pathol Oral Radiol Endod 2007;103 (suppl):1-12.
Yamanaka Y, Yamashita M, Innocentini LMA, Macedo LD, Chahud F, Ribeiro-Silva A, Roselino AM, Rocha MJA, Motta AC. Direct Immunofluorescence as a Helpful Tool for the Differential Diagnosis of Oral Lichen Planus and Oral Lichenoid Lesions. Am J Dermatopathol. 2018;40(7):491-497.
Salgado DS, Jeremias F, Capela MV, et al. Plaque control improves the painful symptoms of oral lichen planus gingival lesions. A short-term study. J Oral Pathol Med. 2013;42: 728-732.
Holmstrup P, Schiøtz AW, Westergaard J. Effect of dental plaque control on gingival lichen planus. Oral Surg Oral Med Oral Pathol.1990;69:585‐590.
Adamo D, Calabria E, Coppola N, Lo Muzio L, Giuliani M, Bizzoca ME, et al. Psychological profile and unexpected pain in oral lichen planus: a case-control multicenter SIPMO study. Oral Dis. 2021 (In press)
González-García A, Diniz-Freitas M, Gándara-Vila P, Blanco-Carrión A, García-García A, Gándara-Rey J. Triamcinolone acetonide mouth rinses for treatment of erosive oral lichen planus: efficacy and risk of fungal over-infection. Oral Dis. 2006;12(6):559-65.
Lodi G, Pellicano R, Carrozzo M. Hepatitis C virus infection and lichen planus: a systematic review with meta-analysis. Oral Diseases. 2010;16:601–12
Gonzalez-Moles MA, Ruiz-Avila I, Rodriguez-Archilla A, Morales-Garcia P, Mesa-Aguado F, Bascones-Martinez A, Bravo M. Treatment of severe erosive gingival lesions by topical application of clobetasol propionate in custom trays. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2003;95(6):688-92.
Gonçalves S., Dionne R.A., Moses G., Carrozzo M. Pharmacotherapeutic Approaches in Oral Medicine. In: Farah C., Balasubramaniam R., McCullough M, (eds). Contemporary Oral Medicine. A comprehensive approach to clinical practice. Springer, Switezerland, 2019.
Carbone M, Goss E, Carrozzo M, et al. Systemic and topical corticosteroid treatment of oral lichen planus: a comparative study with long-term follow-up. J Oral Pathol Med. 2003;32:323‐329.
Eisen D. Hydroxychloroquine sulfate (Plaquenil) improves oral lichen planus: An open trial. J Am Acad Dermatol 1993;28:609–12.
Ho JK, Hantash BM. Systematic review of current systemic treatment options for erosive lichen planus. Expert Rev Dermatol 2012;7:269–82.
Wee JS, Shirlaw PJ, Challacombe SJ, Setterfield JF. Efficacy of mycophenolate mofetil in severe mucocutaneous lichen planus: a retrospective review of 10 patients. Br J Dermatol 2012;167:36–43.
Torti DC, Jorizzo JL, McCarty MA. Oral lichen planus: a case series with emphasis on therapy. Arch Dermatol 2007;143:511–5.
Bruch JM, Treister NS. Immune-Mediated and Allergic Conditions. In: Bruch JM, Treister NS, (eds). Clinical Oral Medicine and Pathology. Humana Press, 2009.
Mignogna MD, Fedele S, Lo Russo L. Dysplasia/neoplasia sur-veillance in oral lichen planus patients: a description of clinical criteria adopted at a single centre and their impact on prognosis. Oral Oncol. 2006;42:819-24.
Ismail SB, Kumar SK, Zain RB. Oral lichen planus and lichenoid reactions: etiopathogenesis, diagnosis, management and malignant transformation. J Oral Sci 2007;49:89–106
Epstein JB, Wan LS, Gorsky M, Zhang L. Oral lichen planus: progress in understanding its malignant potential and the implications for clinical management. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2003;96 (1):32–7.
Elhadad MA, Gaweesh Y. Hawley retainer and lichenoid reaction: a rare case report. BMC Oral Health. 2019 ;19(1):250.
Larsson A, Warfvinge G. Oral lichenoid contact reactions may occasionally transform into malignancy. Eur J Cancer Prevention 2005;14:525-9.
McCartan BE, McCreary CE. Oral lichenoid drug eruptions. Oral Dis 1997;3:58-63.
Den Haute VV, Antoine JL, Lachapelle JM. Histopathological discriminant criteria between lichenoid drug eruption and idiopathic lichen planus: retrospective study on selected samples. Dermatology. 1989;179:10‐13.
Schmidt-Westhausen AM. Oral lichen planus and lichenoid lesions: what’s new? Quintessence Int. 2020;51(2):156-161
Fortuna G, Aria M, Schiavo JH. Drug-induced oral lichenoid reactions: a real clinical entity? A systematic review. Eur J Clin Pharmacol. 2017;73(12):1523-1537.
Warnakulasuriya S. Clinical features and presentation of oral potentially malignant disorders. Oral Surg Oral Med Oral Pathol Oral Radiol. 2018 ;125(6):582-590.
Kuten-Shorrer M, Woo SB, Treister NS. Oral graft-versus-host disease. Dent Clin North Am. 2014;58(2):351-68.