Ovo poglavlje namijenjeno je kao opći uvod u histopatološke dijagnoze odabranih oralnih potencijalno zloćudnih poremećaja (OPZP) za liječnike, kirurge i srodne zdravstvene djelatnike. Očekuje se da će ključni aspekti o kojima se raspravlja u ovom poglavlju pružiti kliničkim zdravstvenim djelatnicima uvid u proces histološke dijagnoze kako bi se kontekstualizirala uloga patologa u multidisciplinarnom upravljanju OPZP-ima. Nije zamišljen kao opsežan tekst i raspravljat će o češćim histološkim značajkama kliničkih OPZP-a, odnosno oralnim lihenoidnim lezijama (OLL) i oralnoj epitelnoj displaziji. Histološke značajke drugih OPMP-a obrađene su na drugom mjestu.
Točna histološka dijagnoza ovisi o kontekstu budući da postoji nekoliko preklapajućih i nespecifičnih mikroskopskih značajki. Neke mikroskopske značajke dobivaju relevantnost u određenim kliničkim kontekstima koji se inače mogu zanemariti kao slučajni. Prije mikroskopske procjene, patolog zahtijeva:
- Istaknuti demografski podaci o pacijentu;
- Klinička povijest i izgled OPZP-a;
- Serološki nalazi (ako je primijenjivo);
- Detalji prethodnih biopsija i, vjerojatno najvažnije;
- Klinička diferencijalna dijagnoza koja uključuje kliničku sumnju na zloćudnu preobrazbu.
To naglašava važnost jasnih i sveobuhvatnih kliničkih informacija na obrascu za patologa koji prati uzorak. Suprotno, kliničari bi uvijek trebali razmatrati izvješće patologa u kliničkom kontekstu; histološka dijagnoza treba nadopunjavati, a ne proturječiti kliničkim zapažanjima. Jasna i otvorena komunikacija između kliničara i patologa podupire učinkovito upravljanje.
Oralne lihenoidne lezije (OLL)
- Različita skupina oralnih upalnih stanja uključujući, ali ne ograničavajući se na, oralni lihen planus (OLP), lihenoidnu reakciju (LR), lupus eritematozus (LE) i bolest transplantata protiv primaoca (GVHD), koji su grupirani zajedno prema svojim zajedničkim histološkim značajkama.
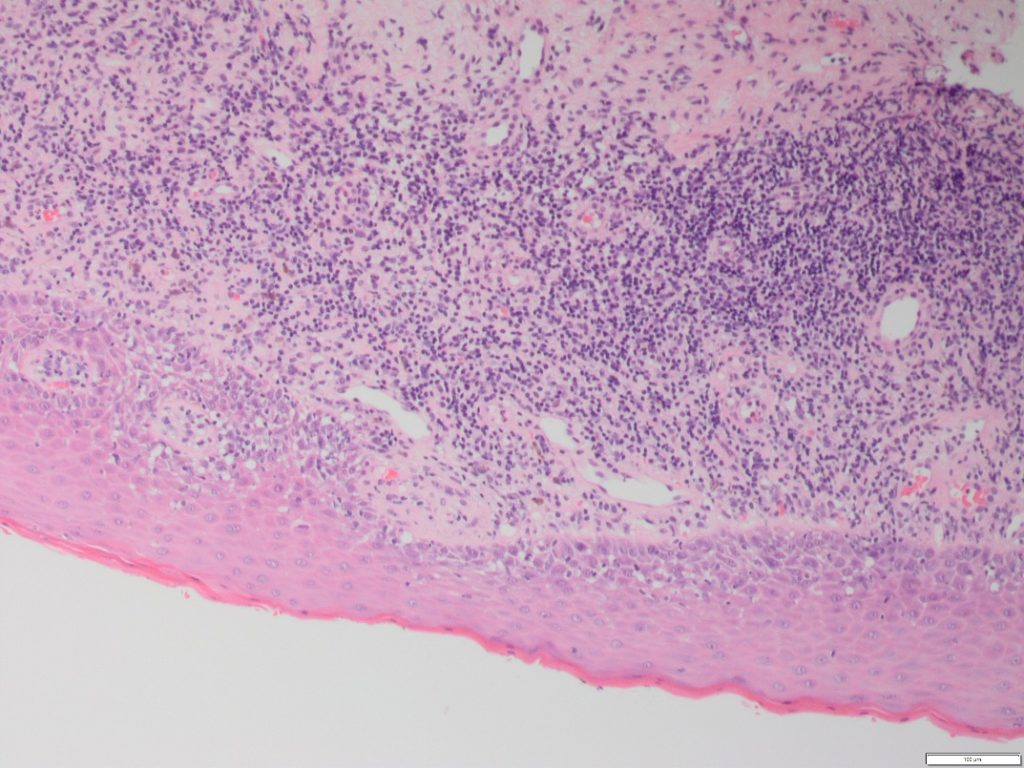
- Pojedinačno viđena u mnogim različitim stanjima, kombinacija hiperkeratoze, degeneracije bazalnih stanica, apoptotičkih (Civatte) tijelešca, subepitelnog upalnog infiltrata i egzostoze limfocita čine histološki temelj za ovu skupinu (slika 1).
- Dodatni nalazi mogu uključivati poremećenu arhitekturu zubaca pile hijalinizaciju bazalne membrane i inkontinenciju pigmenta.
- Važna je promjena u sloju keratina, a ne vrsta ili količina. Sloj keratina može biti orto- ili para-keratin, a opseg može varirati ovisno o mjestu usne šupljine.
- Likvefakcija bazalnih stanica dovodi bazalnih skvamoznih promjena (prividno proširenje trnastog sloja na bazalnu membranu).
- U upalnom infiltratu obično prevladavaju limfociti s vrlo malo plazma stanica osim ako su prisutne ulceracije ili Candida. Tipično je gust i trakasti s različitim stupnjevima ulaženja limfocita u slojeve bazalnih stanica.
- Pokazalo se da analiza histoloških razlika između OLL-a nije značajna, međutim, neke značajke često se smatraju specifičnim za određenu OLL-u.
- Oralna lihenoidna reakcija na lijekove i kontaktna reakcija mogu pokazati mješoviti upalni infiltrat s većom učestalošću plazma stanica. Također se može primijetiti egzocitoza limfocita koja se proteže dalje u suprabazalne slojeve i dublje u laminu propriju s prisutnosšću perivaskularne upale i limfatičnih folikula.
- Hiperplazija zubaca pile u obliku plamena je povezana s LE-om, povremeno dovoljno opsežnim da formira pesudoepiteliomatozne hiperplazije. Duboko keratinsko začepljenje koje se vidi u LE kožnim lezijama nije prisutno u lezijama usne šupljine, međutim može biti prisutno proširenje keratina prema dolje, dajući izgled niske razine keratinizacije.
- Oralni nalaz kod bolesti presatka protiv primaoca može pokazivati identične histološke značajke kao oralni lihen planus. Jedina značajka koja se redovito smatra sugestivnijom za OGVHD je da limfocitni infiltrat nije tako intenzivan i u mnogim slučajevima više ima “izgorjeli” izgled.
- Dva histološka kriterija isključenja za sve oralne lihenoidne lezije su prisutnost displazije kao i prisutnost verukozne epitelne arhitekture.
- OLL kao OPZP-i su dugo kontroverzna tema. Razlog za to je da mnoge displastične lezije pokazuju istodobnu lihenoidnu upalu, a u mnogim lihenoidnim lezijama se ne može točno procijeniti prisutnost displazije zbog promijenjenih slojeva bazalnih stanica i pomiješanog limfocitnog infiltrata. Stoga je bitno uvijek uzeti u obzir prisutnost displazije u bilo kojoj lihenoidnoj leziji.
- Lihenoidna upala također je čest nalaz kod oralne epitelne displazije (OED), posebno u slučajevima koji pokazuju verukozne promjene. Pretpostavlja se da je to vjerojatno kao odgovor na displaziju unutar ovih lezija, a ne kao prava povezanost s temeljnom lihenoidnom lezijom.
- U studiji McParlanda i Warnakulasuriya (2021) o poznatim slučajevima proliferativne verukozne leukoplakije, 59% je dobilo početnu kliničku dijagnozu OLP-a, a 43% biopsija je pokazalo lihenoidne značajke.
Iako OLL-e dijele mnoge kliničko-patološke značajke, njihove su razlike iznimno važne u dijagnozi i samo razumijevanjem kliničke slike uz dodatne nalaze može se postaviti ispravna dijagnoza. Tumačenje histološke procjene nikada se ne smije vršiti bez uvažavanja cjelokupnog kliničkog konteksta.
Oralna submukozna fibroza (OSF)
- Karakteristična histološka značajka oralne submukozne fibroze je prisutnost guste fibroze sa smanjenom vaskularizacijom lamine proprije. Rane lezije mogu biti izazovne za dijagnostiku prije nego što fibroza bude uočljiva. Posebno bojanje, poput Van Giesona, mogu pomoći u vizualizaciji paralelnog rasporeda kolagenih vlakana.
- Hiperkeratoza i epitelna atrofija također su zabilježene kao promjene u epitelu.
- Upalni infiltrat može biti promjenjiv i može čak pokazati lihenoidni upalni uzorak. Važno je da se biopsije procijene na prisutnost epitelne displazije, koja se vidi u do 15% slučajeva
Oralna epitelna displazija (OED)
Svjetska zdravstvena organizacija (SZO) definira OED-u kao ‘spektar stukturalnih i citoloških promjena povezanih s povećanim rizikom od progresije u karcinom pločastih stanica’. Dok se OPZP-e pripisuje kliničkim slikama, OED je histomorfološki definirana. Stoga, uz identifikaciju histoloških značajki povezanih s određenim poremećajima, patolog će također razmotriti prisutnost displazije u bilo kojem biopsijskom uzorku OPZP-a.
- Strukturalne promjene odnose se na poremećenu organizaciju tkiva, dok citološke promjene ukazuju na abnormalnost pojedinih stanica (tablica 1.).
- SZO prepoznaje nekoliko značajki OED-e, ali treba napomenuti da te značajke ostaju subjektivne budući da ne postoje usuglašeni morfometrijski kriteriji.
- Nadalje, kada se uzima izolirano, svaka pojedina značajka također može biti prisutna u reaktivnim stanjima oralne sluznice. Ipak, ove značajke služe kao dijagnostički kriteriji i ističu patologu da lezija može sadržavati potencijal za zloćudnu praobrazbu.
- Uz značajke koje su detaljno opisane u Tablici 1, mnogi bi također dodali verrukoznu površinsku morfologiju, zubce pile ili procese pupanja, spontanu apoptozu u odsutnosti intraepitelnih upalnih stanica, orto- ili para-keratozu s naglim bočnim razgraničenjem i subepitelni limfocitni inflitrat koji oponaša OLL-e.
- Neke skupine također koriste izraz ‘diferencirana displazija’, odnosno širenje suprabazalnog sloja velikim stanicama s obilnom eozinofilnom citoplazmom i međustaničnim edemom. Ove posljednje stukturalne značajke često se pogrešno zamjenjuju za reaktivne hiperplastične promjene.
| Strukturalne promjene | Citološke promjene |
| Nepravilna stratifikacija | Abnormalna varijacija u veličini jezgara |
| Gubitak polariteta bazalnih stanica | Abnormalna varijacija u obliku jezgara |
| Zadebljani zubci pile | Abnormalna varijacija u veličini stanica |
| Povećan broj mitoza | Abnormalna varijacija u obliku stanica |
| Prijevremena keratinizacija u pojedinačnim stanicama | Povećan omjer jezgra:citoplazma |
| Skvamozni vrtlozi unutar zubaca pile | Atipične mitoze |
| Gubitak međustanične kohezije | Povećan broj i veličina nukleola |
| Hiperkromazija |
Table 1. Modificirani SZO morfološki kriteriji OED-e. Morfologija verrukozne površine, podijeljeni zubci pile, spontana apoptoza, naglo razgraničeni uzorak keratoze i opsežna suprabazalna proliferacija također su sve više prihvaćene značajke
Trenutno nema dokaza koji bi ukazivali na to da bi bilo koja pojedinačna značajka trebala imati veće značenje u predviđanju zloćudne preobrazbe. Štoviše, čini se da postoji relativno slaba korelacija između genetskih aberacija i morfoloških promjena. Stoga, prilikom procjene displazije, umjesto primjene bilo kakvog algoritamskog pristupa temeljenog na točkama, patolozi poduzimaju globalni pregled epitelnih promjena, uzimajući u obzir intraoralno podmjesto i njegovu kliničku sliku.
- Postoji pozitivna korelacija između vjerojatnosti i vremena do maligne transformacije s povećanjem stupnjem displazije. Međutim, objavljene prediktivne vrijednosti maligne transformacije imaju široke intervale povjerenja zbog loše reproduktivnosti među promatračima, metodološke heterogenosti i promjenjivih razdoblja praćenja.
- Prediktivne vrijednosti mogu se poboljšati korištenjem analize ploidnosti i gubitka heterozigotnosti kao dodataka histološkom ocjenjivanju, ali one trenutno nisu dostupne izvan visokospecijaliziranih ili istraživačkih centara.
- Budući da je OED-a spektar morfoloških promjena, histološko ocjenjivanje displazije ključno je za informiranje o naknadnom liječenju bilo kojeg OPZP-a.
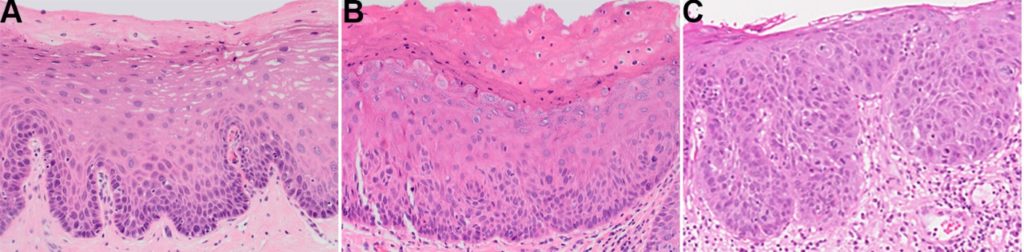
- Većina centara koristi sustav stupnjevanja od tri razine za OED-u, od blage, umjerene i teške displazije (slika 2) pri čemu je karcinom in situ sinonim za tešku displaziju.
- Ovaj sustav djelomično je vođen debljinom epitela u trećinama zahvaćenim strukturalnim i citološkim promjenama. Međutim, treba naglasiti da blaga, umjerena i teška displazija ne moraju nužno biti jednake promjenama ograničenim na bazalnu, srednju i površinsku trećinu epitela. Na primjer, moguće je da se displazija ocijeni kao teška unatoč tome što su promjene ograničene na bazalnu trećinu, naglašavajući kako je stupnjevanje globalna procjena morfoloških promjena.
- Ipak, budući da su granice između svake razine slabo definirane, suboptimalna reproducibilnost među promatračima je složena.
- Kako bi se to prevladalo, neki stručnjaci zagovaraju binarni sustav stupnjevanja (visoki naspram niskog stupnja) i predlažu granične kriterije između stupnjeva.
- U budućnosti bi se reproduktivnost mogla poboljšati ugradnjom platformi umjetne inteligencije.
- U konačnici, cilj bilo kojeg sustava stupnjevanja nije ponovljivost, već informiranje kliničkog upravljanja unutar multidisciplinarnog konteksta.
- Namjera patologa u stupnjevanju trebala bi biti jasna kliničaru bez obzira na korišteni sustav, dodatno naglašavajući potrebu za dobrom multidisciplinarnom suradnjom za učinkovito upravljanje OPZP-ima.
Hyperkeratotic lesions frequently contain concurrent Candida spp. infections. Reaktivni (i stoga reverzibilni) odgovor pločastog epitela na gljivične hife rezultira fenotipskim promjenama koje se ne razlikuju od displazije. U takvim okolnostima, bilo bi mudro razmotriti definitivnu histološko ocjenjivanje OED-je nakon eliminacije infekcije kandidom, ponovne kliničke procjene i/ili ponovne biopsije.
Humani papilomavirus - povezana oralna epitelna displazija (HPV OED)
- Poznato je da je podskup OED-je povezan s visokorizičnim tipovima humanog papiloma virusa (HPV), uglavnom HPV-16.
- Virus inducira donekle jasne histomorfološke promjene epitela, odnosno karioreksu, izolirane suprabazalne apoptotske keratinocite, abortivne mitotičke oblike (mitosoidna tijela) i promjenjive stanice slične koilocitima unutar površinskih slojeva.
- Ove morfološke značajke same po sebi nisu dovoljno specifične da bi potvrdile etiologiju uzrokovanu virusom koja zahtijeva testiranje na transkripcijski aktivan HPV visokog rizika.
- Prisutnost biološki značajnog HPV-a visokog rizika može se dokazati snažnom i difuznom blok pozitivnošću na p16 (često s oštrim bočnim razgraničenjem) nakon čega slijedi in situ hibridizacija za virusnu DNA ili RNA.
- HPV testiranje samo PCR-om, u nedostatku virusnih citopatskih promjena, prema konsenzusu, nije dovoljno specifično za HPV OED-ju.
- Pojedinačni izvještaji o progresiji do karcinoma kod HPV OED-a prijavljeni su u malim serijama slučajeva, ali ukupne stope maligne transformacije trenutno ostaju nepoznate.
- Budući da ne postoji prihvaćeni sustav stuonjevanja, HPV OED bi se za sada trebala stupnjevati i klinički upravljati prema konvencionalnim kriterijima.
Literatura
Alberdi-Navarro, J., et al., Histopathological characterization of the oral lichenoid disease subtypes and the relation with the clinical data. Med Oral Patol Oral Cir Bucal, 2017. 22(3): p. e307-e313.
Arsenic, R. and M.O. Kurrer, Differentiated dysplasia is a frequent precursor or associated lesion in invasive squamous cell carcinoma of the oral cavity and pharynx. Virchows Arch, 2013. 462(6): p. 609-17.
Cai, X., et al., Oral submucous fibrosis: A clinicopathological study of 674 cases in China. J Oral Pathol Med, 2019. 48(4): p. 321-325.
Cheng, Y.S., et al., Diagnosis of oral lichen planus: a position paper of the American Academy of Oral and Maxillofacial Pathology. Oral Surg Oral Med Oral Pathol Oral Radiol, 2016. 122(3): p.
Davidova, L.A., et al., Lichenoid Characteristics in Premalignant Verrucous Lesions and Verrucous Carcinoma of the Oral Cavity. Head Neck Pathol, 2019. 13(4): p. 573-579.
de la Cour, C.D., et al., Human papillomavirus prevalence in oral potentially malignant disorders: Systematic review and meta-analysis. Oral Dis, 2021. 27(3): p. 431-438.
Fitzpatrick, S.G., et al., Histologic lichenoid features in oral dysplasia and squamous cell. Oral Surg Oral Med Oral Pathol Oral Radiol. 2014 Apr;117(4):511-20.
Fonseca-Silva, T., et al., Association between histopathological features of dysplasia in oral leukoplakia and loss of heterozygosity. Histopathology, 2016. 68(3): p. 456-60.
Iocca, O., et al., Potentially malignant disorders of the oral cavity and oral dysplasia: A systematic review and meta-analysis of malignant transformation rate by subtype. Head Neck, 2020. 42(3): p. 539-555.
Lu, R. and G. Zhou, Oral lichenoid lesions: Is it a single disease or a group of diseases? Oral Oncol, 2021. 117: p. 105188.
Khanal, S., et al., Histologic variation in high grade oral epithelial dysplasia when associated with high-risk human papillomavirus. Oral Surg Oral Med Oral Pathol Oral Radiol, 2017. 123(5): p. 566-585.
Kujan, O., et al., Evaluation of a new binary system of grading oral epithelial dysplasia for prediction of malignant transformation. Oral Oncol, 2006. 42(10): p. 987-93.
Lerman, M.A., et al., HPV-16 in a distinct subset of oral epithelial dysplasia. Mod Pathol, 2017. 30(12): p. 1646-1654.
McCord, C., et al., Association of high-risk human papillomavirus infection with oral epithelial dysplasia. Oral Surg Oral Med Oral Pathol Oral Radiol, 2013. 115(4): p. 541-9.
McParland, H. and S. Warnakulasuriya, Lichenoid morphology could be an early feature of oral proliferative verrucous leukoplakia. J Oral Pathol Med, 2021. 50(2): p. 229-235.
Mahmood, H., et al., Use of artificial intelligence in diagnosis of head and neck precancerous and cancerous lesions: A systematic review. Oral Oncol, 2020. 110: p. 104885.
Mehanna, H.M., et al., Treatment and follow-up of oral dysplasia – a systematic review and meta-analysis. Head Neck, 2009. 31(12): p. 1600-9.
Muller, S., Oral lichenoid lesions: distinguishing the benign from the deadly. Mod Pathol. 2017 Jan;30(s1):S54-S67.
Nankivell, P., et al., The binary oral dysplasia grading system: validity testing and suggested improvement. Oral Surg Oral Med Oral Pathol Oral Radiol, 2013. 115(1): p. 87-94.
Nishat, R. and H. Kumar, Collagen fibers in oral submucous fibrosis – A polarizing microscopy study using two special stains. Indian J Pathol Microbiol, 2019. 62(4): p. 537-543.
Odell, E., et al., Oral epithelial dysplasia: recognition, grading and clinical significance. Oral Dis, 2021.
Odell, E.W., et al., Precursor Lesions for Squamous Carcinoma in the Upper Aerodigestive Tract, in Gnepp’s Diagnostic Surgical Pathology of the Head and Neck, D. Gnepp and B.J. A., Editors. 2020, Elsevier.
Odell, E.W., Aneuploidy and loss of heterozygosity as risk markers for malignant transformation in oral mucosa. Oral Dis. 2021 Nov;27(8):1993-2007.
Reibel, J., et al., Oral potentially malignant disorders and oral epithelial dysplasia, in WHO Classification of Head and Neck Tumours 4th edition, World Health Organisation Classification of Tumours, A.K. El Naggar, et al., Editors. 2017, IARC: Lyon, France.
Wils, L.J., et al., Incorporation of differentiated dysplasia improves prediction of oral leukoplakia at increased risk of malignant progression. Mod Pathol, 2020. 33(6): p. 1033-1040.
Woo, S.B., Oral Epithelial Dysplasia and Premalignancy. Head Neck Pathol, 2019. 13(3): p. 423-439.







