Leukoplakija
Predloženo je nekoliko definicija za oralnu leukoplakiju (OL) i one su se kontinuirano razvijale tijekom posljednjih 40 godina (Tablica 1). Najnoviju i široko prihvaćenu definiciju predložio je Suradnički centar SZO za oralni karcinom 2007. godine i ponovno je potvrdio 2020. Leukoplakija je definirana kao „pretežno bijeli plak upitnog rizika koji isključuje (druge) poznate bolesti ili poremećaje koji ne nose povećanu rizik od raka”.
Izraz leukoplakija se koristi kada je isključeno bilo koje drugo stanje oralne sluznice koje se može manifestirati kao bijela lezija (npr. frikcijska keratoza, lihen planus, bijeli spužvasti nevus, vlasasta leukoplakija itd.). Po definiciji leukoplakija je klinički entitet, dijagnoza se isključuje i nema specifičnu patohistološku komponentu.
Epidemiologija i rizični čimbenici za razvoj oralne leukoplakije
Epidemiologija:
- Često se dijagnosticira u bolesnika srednje i starije dobi.
- Češće se identificira u muškaraca.
- OL je šest puta češća među pušačima nego nepušačima.
- Prevalencija OL značajno varira s geografskim varijacijama zbog različitih rizičnih čimbenika, kao što je žvakanje betelovog oraha u jugoistočnoj Aziji.
Rizični čimbenici:
- OL je povezana s različitim rizičnim čimbenicima, sličnim onima uočenim kod raka usne šupljine, kao što su duhan (i dimljeni i bez dima), teška konzumacija alkohola, žvakanje betelovog oraha (posebno u južnoazijskim zemljama) i, za lezije koje zahvaćaju usne, izlaganje ultraljubičastoj (UV) svjetlosti.
- Konzumacija alkohola je neovisni čimbenik rizika. Utvrđeno je da ovi čimbenici mogu imati etiološku ulogu u nastanku OL u više od 75% oboljelih osoba.
Klinički nalaz
- OL može nastati bilo gdje u usnoj šupljini i može zahvaćati jednu ili više lokalizacija. Međutim, u zapadnim industrijaliziranim populacijama najčešća mjesta zahvaćenosti su bočni rub jezika i dno usne šupljine.
- U azijskim populacijama, zbog česte konzumacije betelovog oraha, često su zahvaćene obrazna sluznica i sluznica usana.
- Klinički, leukoplakija pokazuje širok raspon promjenjivih značajki u izgledu (bijela, crvena i pomiješana bijela i crvena, plak/plato granulirana, atrofična), teksturi (glatka, naborana, verukozno granulirana, meka, čvrsta ili tvrda), te veličini i obliku.
- Klinički nalaz oralne leukoplakije može varirati u veličini od relativno male i dobro ograničene lezije do opsežne koja zahvaća veliko područje oralne sluznice.
Leukoplakija se klinički može podijeliti u dvije vrste: homogena i nehomogena. Slike 1 i 2.
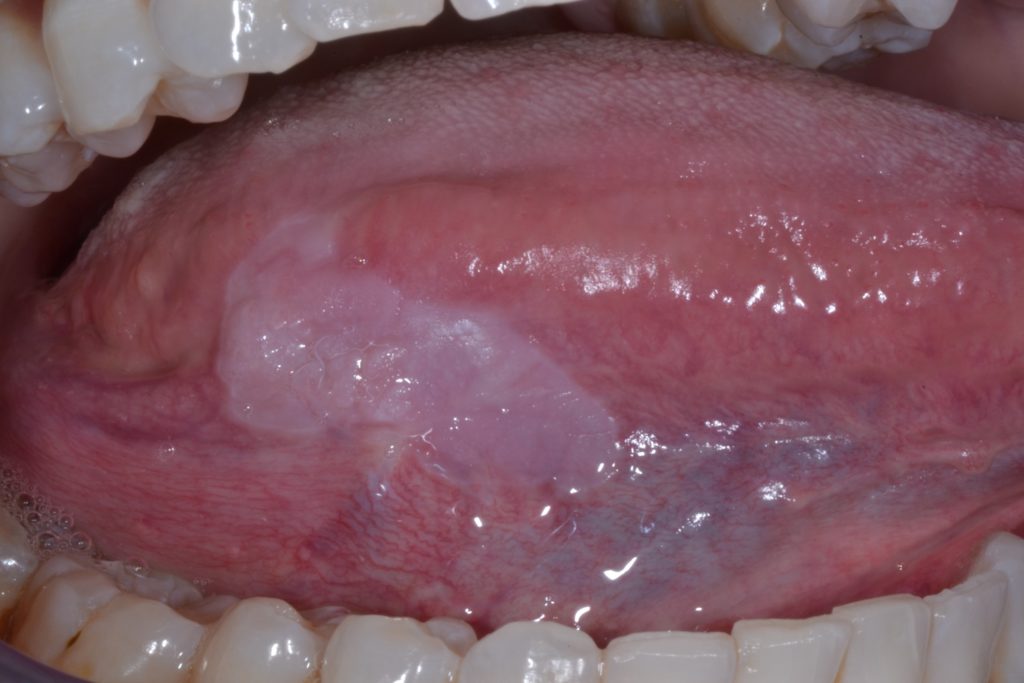
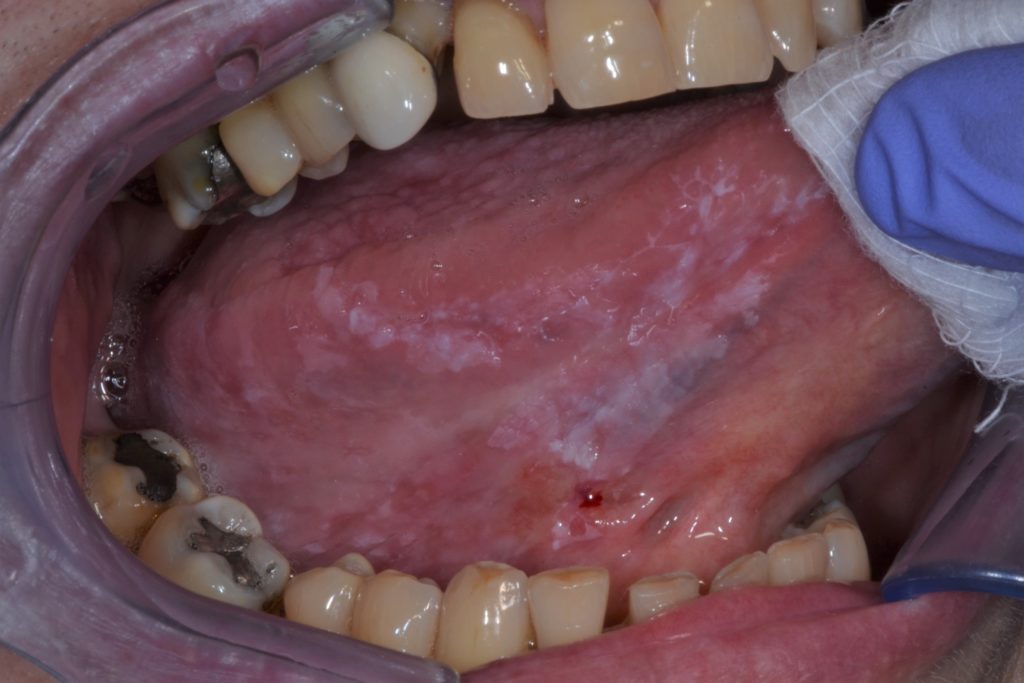
Ova razlika je čisto klinička, temelji se na različitim značajkama kao što su površina, boja i tekstura: homogena leukoplakija i nehomogena leukoplakija (Tablica 2).
| Oralna leukoplakija | |
| Homogena leukoplakija | Nehomogena leukoplakija |
| Ujednačeni ravni i tanki bijeli plak/mrlja s dobro definiranim rubovima, glatka površina povezana s plitkim pukotinama/pukotinama. Ne može se ostrugati. | Pjegasta: miješana bijela i crvena boja Nodularna: male polipoidne izrasline, zaobljene, crvene ili bijele izrasline Verukozna ili egzofitična: naborana ili valovita površina. Ne može se ostrugati. |
Tablica 2: Klasifikacija oralne leukoplakije na temelju različitih kliničkih značajki
Homogena leukoplakija:
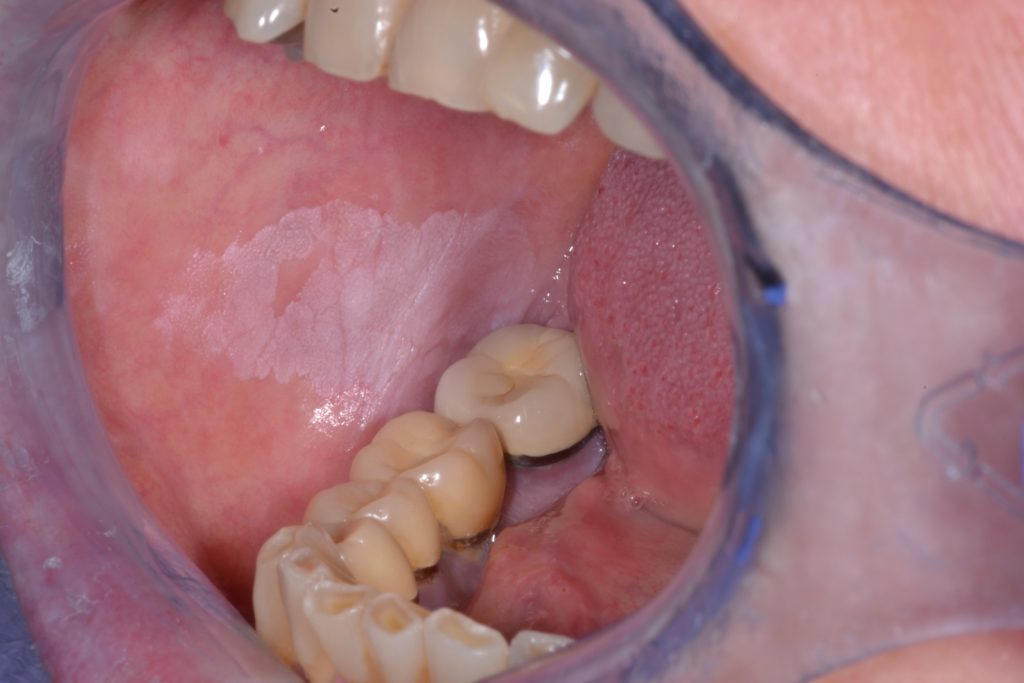
- Karakterizira ju ujednačeni ravni i tanki bijeli plak/mrlja s dobro definiranim rubovima i glatkom površinom koja može biti povezana s plitkim pukotinama/pukotinama površinskog keratina. Dodatno prikazano na slici 3.
Nehomogena leukoplakija:
- Karakterizira ju nepravilna tekstura, koja može uključivati žarišne površinske ulceracije i loše definirane rubove. Nehomogena leukoplakija može biti povezana s različitim kliničkim pojavama koje se koriste za njihov opis: Dodatno ilustrirano na slikama 4 i 5.
- Pjegasta: pomiješana bijela i crvena boja, ali zadržava pretežno bijelu obojenost (također definirana kao eritroleukoplakija)
- Nodularna: male polipozne izbočine, zaobljene, crvene ili bijele izrasline
- Verukozna ili egzofitnična: izgled naborane ili valovite površine
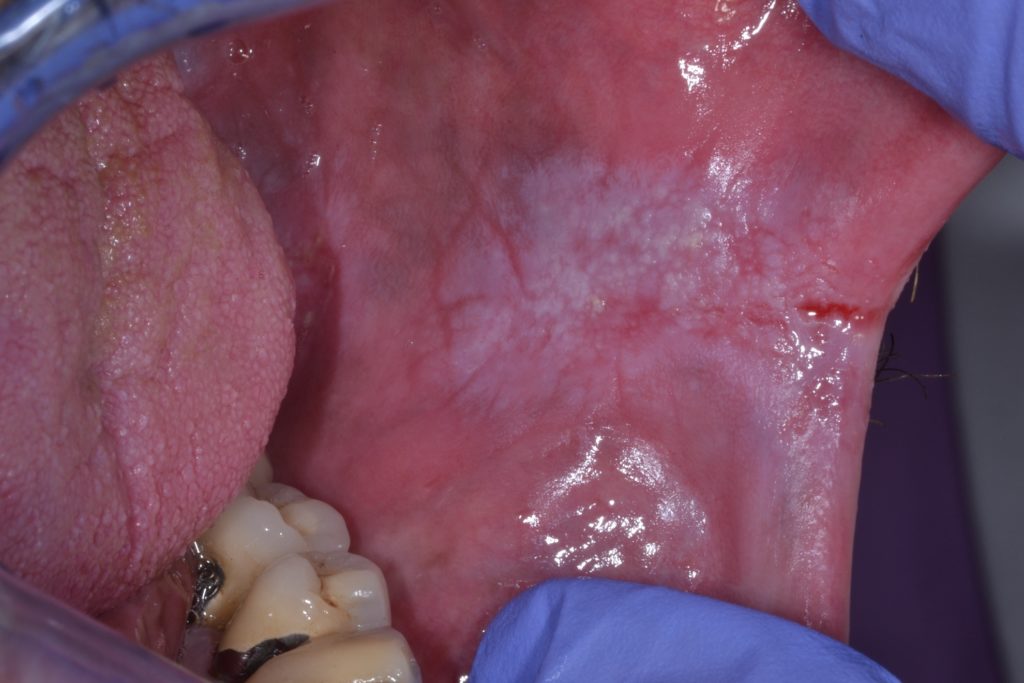
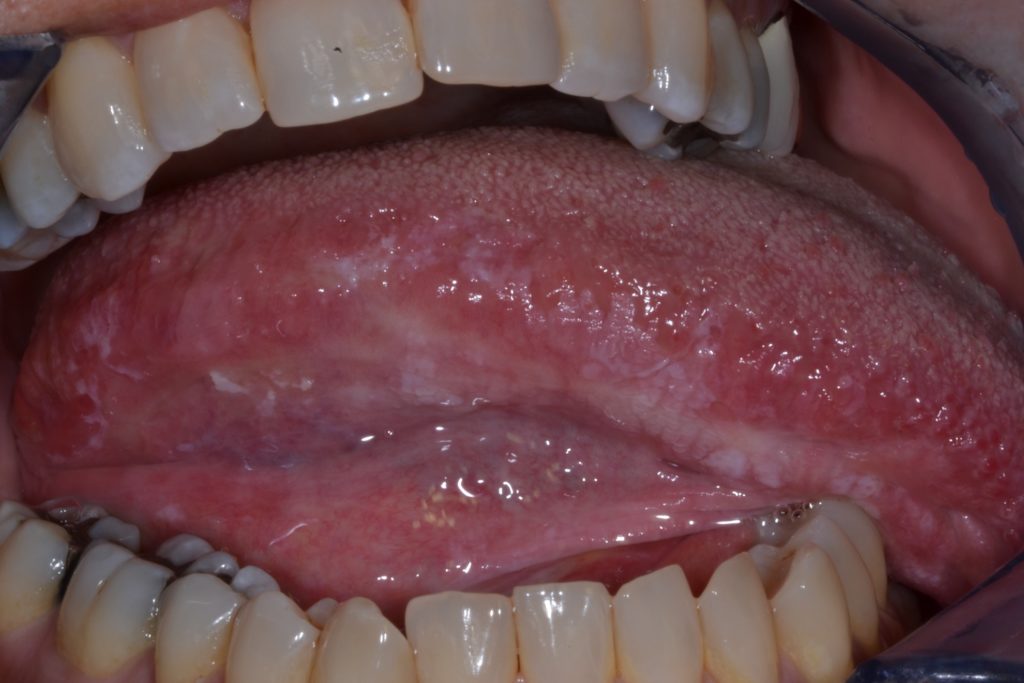
- Leukoplakije su općenito asimptomatske i često se identificiraju tijekom rutinskog pregleda sluznice.
- Homogene leukoplakije su obično asimptomatske.
- Simptomi su rijetki, a ako su prisutni, obično su povezani s nehomogenim oblicima koji mogu pokazati žarišne površinske ulceracije.
- Simptomi koji se češće prijavljuju su nelagoda, trnci i osjetljivost na dodir, tople napitke ili začinjenu hranu.
Rizik od razvoja karcinoma
Oralni karcinom pločastih stanica:
- Oralni karcinom pločastih stanica (OKPS) je najčešća neoplazija koja zahvaća usnu šupljinu.
- OKPS tipično pogađa muškarce starije od 60 godina, međutim, u posljednje vrijeme prevalencija se povećala kod onih mlađih od 40 godina.
- OKPS se može prikazati kao ulceracija koji ne cijeli, rastuća masa s nepravilnom površinom i crvenim ili bijelim lezijama oralnog epitela.
Leukoplakija:
- Leukoplakije su klasificirane kao oralni potencijalno zloćudni poremećaji koji predisponiraju oboljele osobe na povećani rizik od razvoja oralnog karcinoma pločastih stanica.
- OL pokazuje promjenjive postotke progresije u OKPS, koji variraju od 0% do 36,4%. Godišnja stopa transformacije kretala se od 0,3% do 6,9% godišnje, kako je objavljeno u nedavnom preglednom radu observacijskih studija.
- Rizični čimbenici koji su pokazali statističku značajnost za razvoj raka kod osoba zahvaćenih OL-om navedeni su u tablici 4.
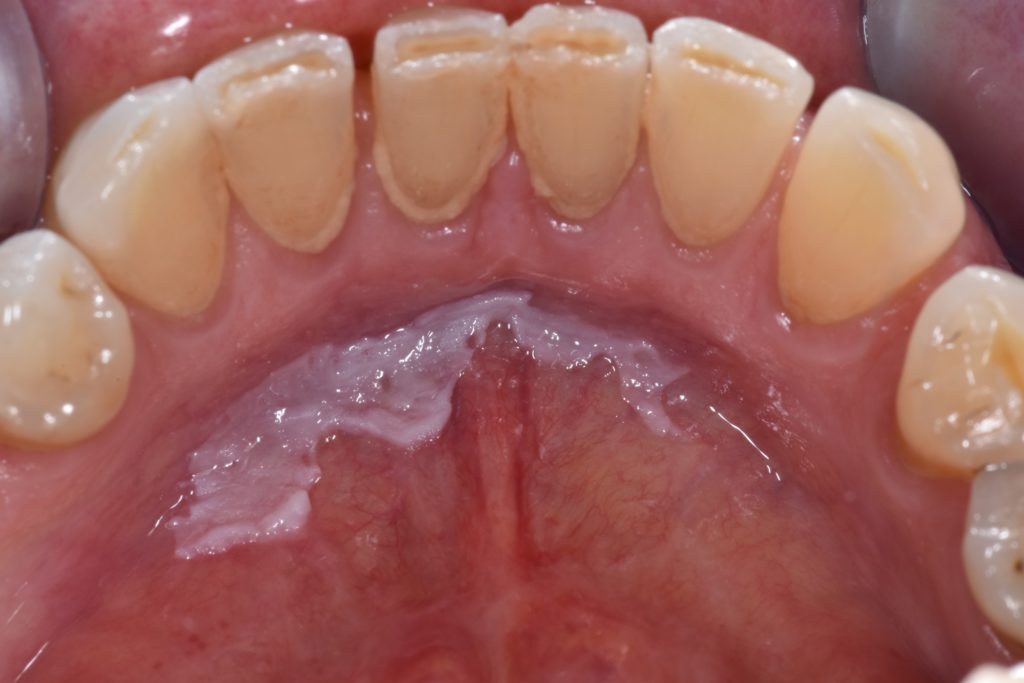
- Slika 6 ilustrira leukoplakiju dna usne šupljne, koje se smatra mjestom visokog rizika zbog nakupljanja kancerogena.
| Oralna leukoplakija – Rizični čimbenici za zloćudnu preobrazbu |
| Nehomogen klinički izgled |
| Ženski spol |
| Dugotrajna leukoplakija |
| Idiopatska leukoplakija (status nepušača/osobe koja ne pije alkohol/ne žvače) |
| Lokalizacija: rub jezika i/ili dno usne šupljine |
| Size > 200 mm2 |
| Prisutnost epitelne displazije |
| Prisutnost Candide albicans (kronična hiperplastična kandidijaza ili kandidijalna leukoplakija) [35] |
Tablica 3. Rizični čimbenici zloćudne preobrazbe oralne leukoplakije
Preobrazba leukoplakije u OKPS:
- Leukoplakije s različitim kliničkim, histološkim ili molekularnim karakteristikama mogu imati različite rizike preobrazbe u OKPS.
- Nehomogene leukoplakije nose veći rizik od razvoja OKPS-a u usporedbi s homogenim leukoplakijama – postoji približno 7 puta veći rizik od zloćudnog razvoja s nehomogenom leukoplakijom u usporedbi s homogenom leukoplakijom i peterostruko povećanje rizika kada je lezija veća od 200 mm2
- U zapadnoj populaciji, starije žene s dugotrajnom idiopatskom leukoplakijom, bez čimbenika rizika, paradoksalno, imaju povećan rizik od progresije u rak vjerojatno zbog endogenog čimbenika rizika, a ne čimbenika okoliša.
- Crvenilo u OL leziji (nehomogena lezija) ukazuje na potencijalnu kolonizaciju od strane gljivica iz roda Candida i također povećani rizik za displaziju i/ili zloćudnu leziju.
- Stupanj displazije, prihvaćen je kao snažan prediktor buduće zloćudne preobrazbe u OL-i i ostaje najbolja pomoć za procjenu rizika od razvoja oralnog karcinoma.
- Nehomogena leukoplakija češće pokazuje tešku displaziju ili površinski invazivni OKPS u vrijeme početne biopsije.
- Rizik od razvoja raka usko je povezan s vrstom lezije i stupnjem displazije.
Dijagnoza leukoplakije
Obavezan je sustavni intraoralni pregled, uz palpaciju vratnih limfnih čvorova [5]. Kao što je gore opisano, pojam leukoplakija je klinička dijagnoza koja isključuje druge klinički prepoznatljive bijele ili bijelo/crvene lezije. Prilikom postavljanja kliničke dijagnoze oralne leukoplakije potrebno je uzeti u obzir sljedeće kriterije:
- bijela mrlja/plak koja se ne može sastrugati
- homogena leukoplakija obično ima dobro razgraničene granice
- nehomogena leukoplakija često ima crvene ili nodularne komponente i difuznije granice
- nema dokaza povezane kronične traumatske iritacije
- ne povlači se nakon eliminacije prividnih traumatskih uzroka
- ne nestaje povlačenjem tkiva
- isključenje drugih bijelih ili bijelo-crvenih lezija
Carrard i van der Waal nedavno su predložili popis parametara, od kojih su neki navedeni u tablici, a koji mogu biti relevantni pri postavljanju kliničke dijagnoze oralne leukoplakije (Tablica 4).
| Značajka | Uloga i važnost tijekom kliničke dijagnoze oralne leukoplakije |
| Dob | OL se rijetko javlja u prva dva desetljeća života |
| Povijest bolesti | Važna za dijagnozu nekoliko bolesti sličnih leukoplakiji, kao što su oralne manifestacije genodermatoza, sifilis i HIV-infekcija. |
| Navike pušenja bilo koje vrste | Češće kod konzumenata duhana |
| Simptomi | Većina OL je asimptomatska, ali se mogu javiti bol ili svrbež. |
| Početak bolesti | OL nastaju polako, tijekom nekoliko mjeseci ili godina. |
| Tijek bolesti | Ima stabilan klinički tijek. |
| Morfologija | |
| Veličina | Veličina nije relevantna s obzirom na kliničku dijagnozu OL. |
| Boja | Boja može varirati od homogene bijele do mješovitog bijelo-crvenog izgleda. |
| Tekstura | Tekstura može varirati od glatke, naborane do verukozne. Ulceracija može ukazivati na malignitet. |
| Otvrdnuće | Palpacija je vrlo važan alat za pregled, a induracija je znak potencijalne zloćudne prirode. |
Tablica 4: Popis nekih značajki, modificiranih od Carrarda i van der Waala, koje mogu biti korisne u kliničkoj dijagnozi i procjeni leukoplakije
- Zlatni standardni postupak za potvrđivanje kliničke dijagnoze oralne leukoplakije je izvođenje reprezentativne incizijske biopsije bijele lezije i slanje tkiva na patohistološku analizu.
- Dijagnostička biopsija je obvezna za potvrdu ili pobijanje dijagnoze OL. Biopsija i naknadni patohistološki pregled omogućuju isključivanje drugih patologija koje se mogu prikazati kao bijela mrlja i procjenu kolonizacije kandide unutar epitela.
- Biopsija je neophodna kako bi se isključila dijagnoza oralnog karcinoma pločastih stanica (OKPS) te za procjenu prisutnosti i stupnja epitelne displazije.
- Patohistološki nalazi povezani s oralnom leukoplakijom mogu varirati od jednostavne epitelne hiperplazije s hiperparakeratozom ili hiper(orto)keratozom, prisutnosti ili odsutnosti i stupnja epitelne displazije.
Iako je predložena binarna klasifikacija za oralnu displaziju (niskog i visokog stupnja), sustav s tri stupnja (blaga, umjerena ili teška) još uvijek se široko koristi u kliničkoj praksi diljem svijeta.
Diferencijalna dijagnoza bijelih mrlja
Tijekom kliničkog pregleda bijele lezije, važno je procijeniti sve potencijalne lokalne traumatske uzroke i, ako se identificira, bijela mrlja treba biti označena kao frikcijska keratoza. Frikcijska keratoza se ne smatra OPZP-om i nakon uklanjanja pretpostavljenog izvora trenja, trebala bi se riješiti.
U sljedećoj tablici nalazi se detaljan popis najvažnijih bijelih lezija i poremećaja koje treba isključiti prije postavljanja kliničke dijagnoze oralne leukoplakije (tablica 5).
| Diferencijalna dijagnoza OL | Opis |
| Bijeli spužvasti nevus | Uočeno u ranom životu, često obiteljska anamneza, obostrana zahvaćenost, često opsežna u ustima, može biti zahvaćena genitalna sluznica. |
| Bijela linija | Dijagnoza je klinička, gotovo uvijek obostrana duž okluzalne ravnine |
| Leukoedem | Klinička dijagnoza obostrane promjene na obraznoj sluznici, nalik velu, a nestaje rastezanjem tkiva. Sklonost među nekim rasnim skupinama: sredovječni tamnoputi ljudi. |
| Fordyceove granule | Mrlje/papule promjera 1-2 mm jasno razgraničene od normalne okolne sluznice; povišene, kružne, bijele ili žuto-bijele boje |
| Morsicatio buccarum | Stanje karakterizirano kroničnom iritacijom ili ozljedom obrazne sluznice, komisura ili obraza, uzrokovano uobičajenim i ponavljanim žvakanjem ili grizenjem. Uočavaju se nepravilne bjelkastožućkaste ljuskice s nazubljenom linijom; često obostrano. |
| Frikcijska keratoza* | Pozitivna klinička anamneza za trenje ili drugu mehaničku traumu. Uglavnom reverzibilna nakon uklanjanja etiološkog uzroka. |
| Keratotične promjene | Uključuju: obrnutu pušačku keratozu, keratozu alveolarnog grebena (KAG), frikcijsku keratozu, keratozu povezanu sa sangvinarijom, keratozu duhanske vrećice i keratozu nepoznatog značaja (KNZ). Obrnuta pušačka keratoza i keratoza duhanske vrećice imaju zloćudni potencijal. |
| Kemijska ozljeda | Povijest produljene izloženosti kemijskom agensu (npr. tableta aspirina) ili kaustičnom agensu (npr. natrijev hipoklorit). Lezija je bolna, ali obično se brzo povlači |
| Nikotinski stomatitis (pušačko nepce) | Sivkasto-bijelo nepce s crvenim mrljama koje se odnose na upaljene male žlijezde slinovnice. Obično je klinička dijagnoza povezana s poviješću pušenja. |
| Uremični stomatitis | Bijeli, oštro omeđeni, adhezivni plakovi fibrinoznog eksudata s nešto oljuštenih epitelnih stanica. Dijagnoza je povezana s pozitivnom anamnezom bubrežne bolesti. |
| Aktinički heilitis | Donja usna je najviše zahvaćeno područje s bijelom lezijom. Tipična klinička slika može varirati i mogu se pojaviti promjene slične leukoplakiji. |
| Oralni lihen planus (OLP) | U tipičnim oblicima bijele papule su spojene linijama da tvore mrežasti izgled na površini promjenjivo upaljene sluznice. Često obostrana zahvaćenost. OLP se također može manifestirati kao deskvamativni gingivitis. Može se pojaviti nekoliko kliničkih podtipova lihen planusa: Retikularni: bijele linije poput čipke Linearni, anularni, papularni: različiti nalazi kao linije, prstenaste ili bijele točkice Plakozni: bijela mrlja sa strijama na rubovimaAtrofični, i ulcerozni: crvene i vidljivo ulceriraneBulozni: vezikularni tip plakoznog lihena može biti vrlo teško razlikovati od oralne leukoplakije. OLP je uvršten u skupinu oralnih potencijalno zloćudnih poremećaja[1] |
| Lihenoidna lezija izravnog kontakta | Uzrokovana produljenim izravnim kontaktom usne sluznice s amalgamom ili drugim vrstama restauracije. Lezija bi trebala nestati u proizvoljno odabranom razdoblju od 2-3 mjeseca nakon uklanjanja nadomjestka. |
| Akutna pseudomembranozna kandidijaza | Općenito raširena infekcija oralne, a ponekad i orofaringealne sluznice. Bijela membrana se može sastrugati ponekad otkrivajući eritematozni/ulcerozni otisak. Povezan s lokalnim (npr. inhalacijski steroidi u spreju) ili sistemskim (npr. imunodeficijencija) podležećim uzrocima. |
| Kronična hiperplastična kandidijaza (Kandidijalna leukoplakija) | Prilijepljena bijela ili bijela i crvena mrlja uzrokovana kroničnom gljivičnom infekcijom, obično Candidom albicans. Uglavnom se nalazi u retro-komisuralnom području, često obostrano. Protugljivični tretman koristi se za procjenu regresije lezija i postavljanje dijagnoze. |
| Vlasasta leukoplakija | Keratoza s okomitim prugama, uzrokovana oportunističkim Epstein Bar virusom, koja je često obostrana i najčešći na bočnim granicama jezika. Povijest imunosupresije zbog HIV-bolesti ili lijekova (npr. nakon transplantacije organa/dugotrajnih steroida). |
| Sifilis, sekundarni | Prilikom postavljanja dijagnoze trebalo bi procijeniti anamnezu i pokazati serološki pozitivan rezultat na Treponemu Pallidum. Klinička slika može biti različita: višestruke “sluzaste mrlje” bjelkaste lihenoidne i promjene na sluznici usne šupljine slične leukoplakiji, višestruke crvene lezije na dorzumu jeziku i nepcu |
| Papilom i lezije povezane s HPV-om (npr. šiljati kondilomi, višežarišna epitelna hiperplazija, obične bradavice) | Dijagnoza se temelji na kliničkom izgledu lezija i na anamnezi. Biopsija, povezana s tipizacijom HPV-a, obično je od pomoći. |
Tablica 5. Detaljan popis glavnih bijelih lezija, stanja ili bolesti koje treba isključiti prije postavljanja kliničke dijagnoze oralne leukoplakije (izmijenjeno prema [1,9])
Liječenje
Primarni cilj u liječenju oralne leukoplakije trebao bi biti praćenje i sprječavanje nastanka oralnog karcinoma. U zajedničkom pokušaju da se smanje šanse za razvoj raka, predložen je niz različitih tretmana i protokola upravljanja. Glavni pristupi u upravljanju OL-om mogu se podijeliti u tri skupine:
- medicinski tretman (lokalni ili sistemski)
- kliničko promatranje (pusti i prati); bez intervencije, ali pod strogim kliničkim i histološkim nadzorom)
- kirurgija: izvodi se različitim tehnikama (skalpel, laserska kirurgija (ekscizija i vaporizacija, kriokirurgija)
Ne postoji konsenzus o najprikladnijem pristupu za OL.
Medicinski tretman
Niti jedan od proučavanih medicinskih i komplementarnih tretmana (vitamin A, beta karoten, bleomicin) nije se pokazao učinkovitim u prevenciji pojave raka kod osoba s OL-om. Nekoliko studija o kemoprevenciji također je pokazalo značajnu toksičnost korištenih lijekova. Medicinsko liječenje leukoplakije može biti učinkovito u smanjenju ili rješenju oralne leukoplakije u kratkom roku, ali je povezano s visokim rizikom od recidiva. Korištenje kemo-preventivnih metoda u klinički kontroliranim ispitivanjima tek treba pokazati svoju učinkovitost u prevenciji zloćudne preobrazbe i kasnijih recidiva.
Pričekaj i gledat (pusti i prati) pristup
Drugi pristup može biti držanje leukoplakije pod strogim kliničkim i histološkim nadzorom, uz česte posjete klinici (pregledi) i biopsije s ciljem što ranijeg otkrivanja zloćudne preobrazbe, čime se osigurava najbolja moguća prognoza. Ovaj pristup temelji se na konceptu “kancerizacije polja”, koji je predložio Slaughter 1957., prema kojem ako je kancerogen doveo do klinički uočljive potencijalno zloćudne ili zloćudne promjene u jednom dijelu usne šupljine, postoji jednak rizik za druge dijelove usne šupljine zbog efekta polja. OL se može smatrati pokazateljem rizika za cijelu oralnu sluznicu, a ne za područje specifično za mjesto. Nedavni RCT procijenio je učinkovitost kirurške ekscizije, u usporedbi sa standardnom njegom u prevenciji OKPS-a u 260 ispitanika s nedisplastičnom OL-om. Dva pacijenta, po jedan u svakoj skupini, razvila su OKPS i autori su zaključili da se redovito kliničko praćenje može smatrati pouzdanim standardom skrbi među pacijentima s nedisplastičnom OL-om.
Kirurško
Postoji jedno randomizirano kontrolirano ispitivanje (RCT) koje je uspoređivalo učinak kirurške ekscizije u odnosu na skupinu bez liječenja ili placeba. Unatoč tome, kirurški tretmani su za većinu kliničara tretman izbora u liječenju oralne leukoplakije. Kirurška ekscizija se često izvodi i postoje neki dokazi koji upućuju na to da to smanjuje rizik od zloćudne preobrazbe u usporedbi s aktivnim nadzorom. Samo podaci iz opservacijskih studija uspoređivali su stope incidencije raka kod ljudi koji su bili ili nisu bili podvrgnuti kirurškom liječenju oralne leukoplakije s razlikama u dijagnostičkim kriterijima i kriterijima uključivanja, intervalima praćenja, karakteristikama sudionika i korištenim kirurškim tehnikama. Ove studije pokazale su vrlo različite rezultate i bile su proturječne u svojim zaključcima.
Kirurška intervencija s ekscizijom hladnim nožem i/ili CO2 laserom obično se izvodi kod nehomogene leukoplakije ili eritroplakije koje su povezane s umjerenom do teškom displazijom.
Zaključak
Kirurgija ostaje opcija liječenja koju većina favorizira, međutim učinkovitost operacije u usporedbi s redovitim kliničkim promatranjem nije procijenjena u RCT-ovima za prevenciju razvoja raka. Do danas je samo jedan RCT usporedio kirurško liječenje s neliječenjem. U nedostatku čvrstih RCT-ova, klinička praksa se i dalje razlikuje.
Reference i daljnje čitanje
Warnakulasuriya, S.; Kujan, O.; Aguirre‐Urizar, J.M.; Bagan, J. V.; González‐Moles, M.Á.; Kerr, A.R.; Lodi, G.; Mello, F.W.; Monteiro, L.; Ogden, G.R.; et al. Oral potentially malignant disorders: A consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2020, odi.13704, doi:10.1111/odi.13704.
van der Waal, I. Oral leukoplakia, the ongoing discussion on definition and terminology. Med. Oral Patol. Oral Cir. Bucal 2015, 20, e685–e692, doi:10.4317/medoral.21007.
Lodi, G.; Franchini, R.; Warnakulasuriya, S.; Varoni, E.M.; Sardella, A.; Kerr, A.R.; Carrassi, A.; Macdonald, L.C.I.; Worthington, H. V. Interventions for treating oral leukoplakia to prevent oral cancer. Cochrane Database Syst. Rev. 2016.
Amagasa, T.; Yamashiro, M.; Uzawa, N. Oral premalignant lesions: From a clinical perspective. Int. J. Clin. Oncol. 2011, 16, 5–14, doi:10.1007/s10147-010-0157-3.
Warnakulasuriya, S. Clinical features and presentation of oral potentially malignant disorders. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018, 125, 582–590.
Staines, K.; Rogers, H. Oral leukoplakia and proliferative verrucous leukoplakia: A review for dental
Speight, P.M.; Khurram, S.A.; Kujan, O. Oral potentially malignant disorders: risk of progression to malignancy. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018.
Napier, S.S.; Speight, P.M. Natural history of potentially malignant oral lesions and conditions: An overview of the literature. J. Oral Pathol. Med. 2008, 37, 1–10.
Carrard, V.; van der Waal, I. A Clinical Diagnosis of Oral Leukoplakia . Med Oral Patol Oral Cir Bucal 2018.
Sundberg, J.; Korytowska, M.; Holmberg, E.; Bratel, J.; Wallström, M.; Kjellström, E.; Blomgren, J.; Kovács, A.; Öhman, J.; Sand, L.; et al. Recurrence rates after surgical removal of oral leukoplakia-A prospective longitudinal multicentre study. PLoS One 2019, 14, doi:10.1371/journal.pone.0225682.
Petti, S. Pooled estimate of world leukoplakia prevalence: A systematic review. Oral Oncol. 2003,
Villa, A.; Sonis, S. Oral leukoplakia remains a challenging condition. Oral Dis. 2018, 24, 179–183, doi:10.1111/odi.12781.
Mello, F.W.; Miguel, A.F.P.; Dutra, K.L.; Porporatti, A.L.; Warnakulasuriya, S.; Guerra, E.N.S.; Rivero, E.R.C. Prevalence of oral potentially malignant disorders: A systematic review and
Jayasooriya, P.R.; Dayaratne, K.; Dissanayake, U.B.; Warnakulasuriya, S. Malignant transformation of oral leukoplakia: a follow-up study. Clin. Oral Investig. 2020, doi:10.1007/s00784-020-03322-4.
Warnakulasuriya, S. Oral potentially malignant disorders: A comprehensive review on clinical aspects and management. Oral Oncol. 2020, 102, doi:10.1016/j.oraloncology.2019.104550.
Arduino, P.; Bagan, J.; El-Naggar, A.; Carrozzo, M. Urban legends series: Oral leukoplakia. Oral Dis. 2013, 19, 642–659.
Villa, A.; Celentano, A.; Glurich, I.; Borgnakke, W.S.; Jensen, S.B.; Peterson, D.E.; Delli, K.; Ojeda, D.; Vissink, A.; Farah, C.S. World Workshop on Oral Medicine VII: Prognostic biomarkers in oral leukoplakia: A systematic review of longitudinal studies. Oral Dis. 2019, 25, 64–78.
Villa, A.; Woo, S. Bin Leukoplakia—A Diagnostic and Management Algorithm. J. Oral Maxillofac. Surg. 2017, 75, 723–734.
Syrjänen, S.; Lodi, G.; von Bültzingslöwen, I.; Aliko, A.; Arduino, P.; Campisi, G.; Challacombe, S.; Ficarra, G.; Flaitz, C.; Zhou, H.; et al. Human papillomaviruses in oral carcinoma and oral potentially malignant disorders: A systematic review. Oral Dis. 2011, 17, 58–72, doi:10.1111/j.1601-0825.2011.01792.x.
Varoni, E.M.; Lombardi, N.; Franchini, R.; D’Amore, F.; Noviello, V.; Cassani, B.; Moneghini, L.; Sardella, A.; Lodi, G. Oral Human Papillomavirus (HPV) and sexual behaviors in a young cohort of oral cancer survivors. Oral Dis. 2020, odi.13622, doi:10.1111/odi.13622.
Awadallah, M.; Idle, M.; Patel, K.; Kademani, D. Management update of potentially premalignant oral epithelial lesions. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018, 125, 628–636.
Warnakulasuriya, S.; Johnson, N.W.; Van Der Waal, I. Nomenclature and classification of potentially malignant disorders of the oral mucosa. J. Oral Pathol. Med. 2007, 36, 575–580.
van der Waal, I. Potentially malignant disorders of the oral and oropharyngeal mucosa; present concepts of management. Oral Oncol. 2010, 46, 423–425.
Pentenero, M.; Meleti, M.; Vescovi, P.; Gandolfo, S. Oral proliferative verrucous leucoplakia: Are there particular features for such an ambiguous entity? A systematic review. Br. J. Dermatol. 2014, 170, 1039–1047.
Lombardi, N.; D’amore, F.; Elli, C.; Pispero, A.; Moneghini, L.; Franchini, R. Gingival lesion in proliferative verrucous leukoplakia. Dent. Cadmos 2020, 88, 647–648, doi:10.19256/d.cadmos.10.2020.03.
Hansen, L.S.; Olson, J.A.; Silverman, S. Proliferative verrucous leukoplakia. A long-term study of thirty patients. Oral Surgery, Oral Med. Oral Pathol. 1985, doi:10.1016/0030-4220(85)90313-5.
Villa, A.; Menon, R.S.; Kerr, A.R.; De Abreu Alves, F.; Guollo, A.; Ojeda, D.; Woo, S.B. Proliferative leukoplakia: Proposed new clinical diagnostic criteria. Oral Dis. 2018, 24, 749–760,
Aguirre-Urizar, J.M. Proliferative multifocal leukoplakia better name that proliferative verrucous leukoplakia. World J. Surg. Oncol. 2011, 9.
Lombardi, N.; Varoni, E.M.; Moneghini, L.; Lodi, G. Submucosal oral squamous cell carcinoma of the tongue. Oral Oncol. 2020, 105121, doi:10.1016/j.oraloncology.2020.105121.
Lodi, G.; Tarozzi, M.; Baruzzi, E.; Costa, D.; Franchini, R.; D’Amore, F.; Carassi, A.; Lombardi, N. Odontoiatria e cancro della bocca: dai fattori di rischio alla riabilitazione – Modulo 1: Epidemiologia e fattori di rischio. Dent. Cadmos 2021, 89, 01, doi:10.19256/d.cadmos.01.2021.14.
Lombardi, N.; Sorrentino, D.; D’amore, F.; Moneghini, L.; Franchini, R.; Sardella, A. Oral erythroleukoplakia on the lateral border of the tongue in a young patient. Dent. Cadmos 2020, 88, 277–278, doi:10.19256/d.cadmos.05.2020.03.
Warnakulasuriya, S.; Ariyawardana, A. Malignant transformation of oral leukoplakia: A systematic review of observational studies. J. Oral Pathol. Med. 2016, 45, 155–166, doi:10.1111/jop.12339.
Ho, M.W.; Risk, J.M.; Woolgar, J.A.; Field, E.A.; Field, J.K.; Steele, J.C.; Rajlawat, B.P.; Triantafyllou, A.; Rogers, S.N.; Lowe, D.; et al. The clinical determinants of malignant transformation in oral epithelial dysplasia. Oral Oncol. 2012, 48, 969–976, doi:10.1016/j.oraloncology.2012.04.002.
Field, E.A.; McCarthy, C.E.; Ho, M.W.; Rajlawat, B.P.; Holt, D.; Rogers, S.N.; Triantafyllou, A.; Field, J.K.; Shaw, R.J. The management of oral epithelial dysplasia: The Liverpool algorithm. Oral Oncol. 2015, 51, 883–887.
van der Waal, I. Potentially malignant disorders of the oral and oropharyngeal mucosa; terminology, classification and present concepts of management. Oral Oncol. 2009.
Diz P, Gorsky M, Johnson NW, Kragelund C, Manfredi M, Odell E, et al. Oral leukoplakia and erythroplakia: a protocol for diagnosis and management. EAOM – Diagnostic Ther. Protoc. 2011, 1, 1-8.
Van der Waal, I.; Axéll, T. Oral leukoplakia: A proposal for uniform reporting. Oral Oncol. 2002, 38, 521–526.
Reddi, S.P.; Shafer, A.T. Oral Premalignant Lesions: Management Considerations. Oral Maxillofac. Surg. Clin. North Am. 2006, 18, 425–433.
Pereira, J.D.S.; Carvalho, M.D.V.; Henriques, Á.C.G.; De Queiroz Camara, T.H.; Miguel, M.C.D.C.; Freitas, R.D.A. Epidemiology and correlation of the clinicopathological features in oral epithelial dysplasia: Analysis of 173 cases. Ann. Diagn. Pathol. 2011, 15, 98–102, doi:10.1016/j.anndiagpath.2010.08.008.
Rock, L.D.; Rosin, M.P.; Zhang, L.; Chan, B.; Shariati, B.; Laronde, D.M. Characterization of epithelial oral dysplasia in non-smokers: First steps towards precision medicine. Oral Oncol. 2018, 78, 119–125, doi:10.1016/j.oraloncology.2018.01.028.
Dilhari, A.; Weerasekera, M.M.; Siriwardhana, A.; Maheshika, O.; Gunasekara, C.; Karunathilaka, S.; Nagahawatte, A.; Fernando, N. Candida infection in oral leukoplakia: an unperceived public health problem. Acta Odontol. Scand. 2016, 74, 565–569, doi:10.1080/00016357.2016.1220018.
Speight, P.M. Update on oral epithelial dysplasia and progression to cancer. Head Neck Pathol. 2007, 1, 61–66, doi:10.1007/s12105-007-0014-5.
Warnakulasuriya, S.; Kovacevic, T.; Madden, P.; Coupland, V.H.; Sperandio, M.; Odell, E.; Møller, H. Factors predicting malignant transformation in oral potentially malignant disorders among patients accrued over a 10-year period in South East England. J. Oral Pathol. Med. 2011, 40, 677–683, doi:10.1111/j.1600-0714.2011.01054.x.
Arduino, P.G.; Surace, A.; Carbone, M.; Elia, A.; Massolini, G.; Gandolfo, S.; Broccoletti, R. Outcome of oral dysplasia: A retrospective hospital-based study of 207 patients with a long follow-up. J. Oral Pathol. Med. 2009, 38, 540–544, doi:10.1111/j.1600-0714.2009.00782.x.
Watabe, Y.; Nomura, T.; Onda, T.; Yakushiji, T.; Yamamoto, N.; Ohata, H.; Takano, N.; Shibahara, T. Malignant transformation of oral leukoplakia with a focus on low-grade dysplasia. J. Oral Maxillofac. Surgery, Med. Pathol. 2016, 28, 26–29, doi:10.1016/j.ajoms.2015.02.007.
Kujan, O.; Oliver, R.J.; Khattab, A.; Roberts, S.A.; Thakker, N.; Sloan, P. Evaluation of a new binary system of grading oral epithelial dysplasia for prediction of malignant transformation. Oral Oncol. 2006, doi:10.1016/j.oraloncology.2005.12.014.
El-Naggar A.K., Chan J.K.C., Grandis J.R., Takata T., S.P.J. WHO classification of Head and Neck tumors; 4th ed.; IARC Press: Lyon, 2017; ISBN 9789283224372.
Thomson, P. Oral Precancer; Thomson, P., Ed.; John Wiley & Sons, Ltd.: West Sussex, UK, 2012; ISBN 9781118702840.
Warnakulasuriya, S.; Reibel, J.; Bouquot, J.; Dabelsteen, E. Oral epithelial dysplasia classification systems: Predictive value, utility, weaknesses and scope for improvement. J. Oral Pathol. Med. 2008, 37, 127–133.
Pentenero, M.; Carrozzo, M.; Pagano, M.; Galliano, D.; Broccoletti, R.; Scully, C.; Gandolfo, S. Oral mucosal dysplastic lesions and early squamous cell carcinomas: Underdiagnosis from incisional biopsy. Oral Dis. 2003, 9, 68–72, doi:10.1034/j.1601-0825.2003.02875.x.
Lee, J.J.; Hung, H.C.; Cheng, S.J.; Chen, Y.J.; Chiang, C.P.; Liu, B.Y.; Jeng, J.H.; Chang, H.H.; Kuo, Y.S.; Lan, W.H.; et al. Carcinoma and dysplasia in oral leukoplakias in Taiwan: Prevalence and risk factors. Oral Surgery, Oral Med. Oral Pathol. Oral Radiol. Endodontology 2006, 101, 472–480, doi:10.1016/j.tripleo.2005.07.024.
Cabay, R.J.; Morton, T.H.; Epstein, J.B. Proliferative verrucous leukoplakia and its progression to oral carcinoma: A review of the literature. J. Oral Pathol. Med. 2007, 36, 255–261, doi:10.1111/j.1600-0714.2007.00506.x.
Iocca, O.; Sollecito, T.P.; Alawi, F.; Weinstein, G.S.; Newman, J.G.; De Virgilio, A.; Di Maio, P.; Spriano, G.; Pardiñas López, S.; Shanti, R.M. Potentially malignant disorders of the oral cavity and oral dysplasia: A systematic review and meta-analysis of malignant transformation rate by subtype. Head Neck 2020, 42, 539–555.
Bagan, J.; Murillo-Cortes, J.; Poveda-Roda, R.; Leopoldo-Rodado, M.; Bagan, L. Second primary tumors in proliferative verrucous leukoplakia: a series of 33 cases. Clin. Oral Investig. 2020, 24, 1963–1969, doi:10.1007/s00784-019-03059-9.
Reibel, J.; Gale, N.; Hille, J.; Hunt, J.; Lingen, M.; Muller, S.; Sloan, P.; Tilakaratne, W.; Westra, W.; Williams, M.; et al. Oral potentially malignant disorders and oral epithelial dysplasia. In WHO classification of head and neck tumours; IARC, Ed.; Lyon France, 2017; pp. 112–115 ISBN 9789283224389.
Ranganathan, K.; Kavitha, L. Oral epithelial dysplasia: Classifications and clinical relevance in risk assessment of oral potentially malignant disorders. J. Oral Maxillofac. Pathol. 2019, 23, 19–27.
Barnes, L.; Eveson, J.W.; Reichart, P.; Sidransky, D. World Health Organization Classification of Tumours. Pathology & Genetics. Head and Neck Tumours. International Agency for Research on Cancer (IARC). WHO Classif. Tumours (3rd Ed. 2005, 177–80.
Lee, J.J.; Hung, H.C.; Cheng, S.J.; Chiang, C.P.; Liu, B.Y.; Yu, C.H.; Jeng, J.H.; Chang, H.H.; Kok, S.H. Factors associated with underdiagnosis from incisional biopsy of oral leukoplakic lesions. Oral Surgery, Oral Med. Oral Pathol. Oral Radiol. Endodontology 2007, 104, 217–225, doi:10.1016/j.tripleo.2007.02.012.
Meleti, M.; Giovannacci, I.; Vescovi, P.; Pedrazzi, G.; Govoni, P.; Magnoni, C. Histopathological determinants of autofluorescence patterns in oral carcinoma. Oral Dis. 2020, doi:10.1111/odi.13304.
Tiwari, L.; Kujan, O.; Farah, C.S. Optical fluorescence imaging in oral cancer and potentially malignant disorders: A systematic review. Oral Dis. 2020.
Warnakulasuriya, S. White, red, and mixed lesions of oral mucosa: A clinicopathologic approach to diagnosis. Periodontol. 2000 2019, 80, 89–104.
Auluck, A.; Pai, K.M. (Mis)interpretations of leukoplakia. J. Can. Dent. Assoc. (Tor). 2005.
Müller, S. Frictional Keratosis, Contact Keratosis and Smokeless Tobacco Keratosis: Features of Reactive White Lesions of the Oral Mucosa. Head Neck Pathol. 2019, 13, 16–24.
Kramer, I.R.; El, L.; Lee, K.W. The clinical features and risk of malignant transformation in sublingual keratosis. Br. Dent. J. 1978, 144, 171–180, doi:10.1038/sj.bdj.4804055.
Eversole, L.R.; Eversole, G.M.; Kopcik, J. Sanguinaria-associated oral leukoplakia: Comparison with other benign and dysplastic leukoplakic lesions. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod. 2000, 89, 455–464, doi:10.1016/S1079-2104(00)70125-9.
Gupta, P.C.; Mehta, F.S.; Daftary, D.K. Incidence rates of oral cancer and natural history of oral precancerous lesions in a 10-year follow-up study of Indian villagers. Community Dent. Oral Epidemiol. 1980, 8, 287–333, doi:10.1111/j.1600-0528.1980.tb01302.x.
Sreenivasa Bharath, T.; Govind Raj Kumar, N.; Nagaraja, A.; Saraswathi, T.R.; Suresh Babu, G.; Ramanjaneya Raju, P. Palatal changes of reverse smokers in a rural coastal Andhra population with review of literature. J. Oral Maxillofac. Pathol. 2015, 19, 182–187, doi:10.4103/0973-029X.164530.
Woo, S. Bin; Grammer, R.L.; Lerman, M.A. Keratosis of unknown significance and leukoplakia: A preliminary study. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2014, 118, 713–724, doi:10.1016/j.oooo.2014.09.016.
Villa, A.; Hanna, G.J.; Kacew, A.; Frustino, J.; Hammerman, P.S.; Woo, S. Bin Oral keratosis of unknown significance shares genomic overlap with oral dysplasia. Oral Dis. 2019, 25, 1707–1714, doi:10.1111/odi.13155.
Lodi, G.; Porter, S. Management of potentially malignant disorders: Evidence and critique. J. Oral Pathol. Med. 2008, 37, 63–69.
Kanatas, A.N.; Fisher, S.E.; Lowe, D.; Ong, T.K.; Mitchell, D.A.; Rogers, S.N. The configuration of clinics and the use of biopsy and photography in oral premalignancy: A survey of consultants of the British Association of Oral and Maxillofacial Surgeons. Br. J. Oral Maxillofac. Surg. 2011, 49, 99–105, doi:10.1016/j.bjoms.2010.01.016.
Kumar, A.; Cascarini, L.; McCaul, J.A.; Kerawala, C.J.; Coombes, D.; Godden, D.; Brennan, P.A. How should we manage oral leukoplakia? Br. J. Oral Maxillofac. Surg. 2013, 51, 377–383, doi:10.1016/j.bjoms.2012.10.018.
Dionne, K.R.; Warnakulasuriya, S.; Zain, R.B.; Cheong, S.C. Potentially malignant disorders of the oral cavity: Current practice and future directions in the clinic and laboratory. Int. J. Cancer 2015, 136, 503–515.
Diajil, A.; Robinson, C.M.; Sloan, P.; Thomson, P.J. Clinical Outcome Following Oral Potentially Malignant Disorder Treatment: A 100 Patient Cohort Study. Int. J. Dent. 2013, 2013, 1–8, doi:10.1155/2013/809248.
Ribeiro, A.S.; Salles, P.R.; da Silva, T.A.; Mesquita, R.A. A Review of the Nonsurgical Treatment of Oral Leukoplakia. Int. J. Dent. 2010, 2010, 1–10, doi:10.1155/2010/186018.
Jaiswal, G.; Jaiswal, S.; Kumar, R.; Sharma, A. Field cancerization: concept and clinical implications in head and neck squamous cell carcinoma. J. Exp. Ther. Oncol. 2013.
Arduino, P.G.; Lodi, G.; Cabras, M.; Macciotta, A.; Gambino, A.; Conrotto, D.; Karimi, D.; El Haddad, G.; Carbone, M.; Broccoletti, R. A Randomized Controlled Trial on Efficacy of Surgical Excision of non-dysplastic Leukoplakia to Prevent Oral Cancer. Cancer Prev. Res. 2020, canprevres.0234.2020, doi:10.1158/1940-6207.capr-20-0234.
Mehanna, H.M.; Rattay, T.; Smith, J.; McConkey, C.C. Treatment and follow-up of oral dysplasia – A systematic review and meta-analysis. Head Neck 2009, doi:10.1002/hed.21131.
Saito, T.; Sugiura, C.; Hirai, A.; Notani, K.I.; Totsuka, Y.; Shindoh, M.; Fukuda, H. Development of squamous cell carcinoma from pre-existent oral leukoplakia: With respect to treatment modality. Int. J. Oral Maxillofac. Surg. 2001, 30, 49–53.
Zhang, L.; Lubpairee, T.; Laronde, D.M.; Rosin, M.P. Should severe epithelial dysplasia be treated? Oral Oncol. 2016, 60, 125–129, doi:10.1016/j.oraloncology.2016.07.007.
Balasundaram, I.; Payne, K.F.B.; Al-Hadad, I.; Alibhai, M.; Thomas, S.; Bhandari, R. Is there any benefit in surgery for potentially malignant disorders of the oral cavity? J. Oral Pathol. Med. 2014.
Thomson, P.J.; McCaul, J.A.; Ridout, F.; Hutchison, I.L. To treat…or not to treat? Clinicians’ views on the management of oral potentially malignant disorders. Br. J. Oral Maxillofac. Surg. 2015, 53, 1027–1031, doi:10.1016/j.bjoms.2015.08.263.
Kuribayashi, Y.; Tsushima, F.; Morita, K.; Matsumoto, K.; Sakurai, J.; Uesugi, A.; Sato, K.; Oda, S.; Sakamoto, K.; Harada, H. Long-term outcome of non-surgical treatment in patients with oral leukoplakia. Oral Oncol. 2015, 51, 1020–1025, doi:10.1016/j.oraloncology.2015.09.004.
Mogedas-Vegara, A.; Hueto-Madrid, J.A.; Chimenos-Küstner, E.; Bescós-Atín, C. Oral leukoplakia treatment with the carbon dioxide laser: A systematic review of the literature. J. Cranio-Maxillofacial Surg. 2016, doi:10.1016/j.jcms.2016.01.026.







