Oralna submukozna fibroza (OSF) je kronično, progresivno ožiljno stanje koje utječe na sluznicu orofarinksa, a često i na gornji dio jednjaka.
Ne postoji univerzalno prihvaćena definicija OSF, a novije definicije imaju za cilj dati komentar na etiologiju, epidemiologiju i kliničke značajke bolesti. Pindborg je 1966. definirao OSF kao “podmuklu, kroničnu bolest koja zahvaća bilo koji dio usne šupljine, a ponekad i ždrijela”. Brad (2019) definira OSF kao „kronično, prekancerozno i često iscrpljujuće stanje karakterizirano sporo progresivnom fibrozom usne šupljine i orofarinksa”, a Langdon (2007) je opisao OSF kao „progresivnu bolest u kojoj se fibrozne trake formiraju ispod oralne sluznice”.
Etiopatogeneza
Etiologija OSF je višeuzročna.
- Areka ili betelov orah je naziv za orašasti plod koji potječe od biljke Areca.
- U razvoju OSF zabilježen je odnos ovisan o dozi za učestalost i trajanje žvakanja.
- Žvakanje areke, betela ili paana uobičajena je rekreativna navika na indijskom potkontinentu, a njihova konzumacija postaje sve češća u zapadnim zajednicama zbog migracije.
- Određeni pripravci orašastih plodova areke uključuju duhan i druge poznate karcinogene. Sam za sebe, areka orah je priznati kancerogen jer sadrži određene tanine i alkaloide koji su citotoksični i genotoksični. Gašeno vapno, koje je još jedan uobičajeni sastojak u pripravcima od orašastih plodova areke, ima povišene koncentracije arsena.
- U hinduističkoj religiji, areka orah smatra se božanskim i konzumira se zbog uočene medicinske vrijednosti. Također se doživljava kao afrodizijak, sredstvo koje poboljšava oralnu higijenu i smanjuje zadah iz usta, stimulans sline koji poboljšava probavu, a unutar indijskog potkontinenta vjeruje se da ima stabilizirajući učinak na kontrolu glikemije u bolesnika s dijabetesom.
- Arekolin, nusprodukt metabolizma areka orašastih plodova, alkaloid je koji lako prolazi krvno-moždanu barijeru i uključen je u potencijal ovisnosti kod navike žvakanja areka orašastih plodova. Posljednji fiziološki učinci često se opisuju kao euforični, korisnici također opisuju povećanu svijest i poboljšanu produktivnost.
- Žvakanje areka orašastih plodova prepoznato je kao etiološki čimbenik u razvoju OSF. Međunarodna agencija za istraživanje raka kategorizirala je areka orah kao kancerogen prve skupine.
- Ostali prijavljeni etiološki čimbenici uključuju već postojeću naviku pušenja (bez dima), hematooške deficijencije, anemiju i pothranjenost.
- Može postojati i genetska predispozicija, povezana s određenim HLA podtipovima i haplotipovima (A10/DR3).
- Pothranjenost, anemija i hematološke deficijencije povezani su s atrofijom oralne sluznice i povećanim potencijalom za sintezu kolagena.
Žvakanje areka orašastih plodova glavni je etiološki čimbenik rizika u razvoju OSF dok se gore navedeni čimbenici mogu smatrati doprinosećima.
Histopatologija
- OSF je karakterizirana abnormalnim odlaganjem kolagena.
- Areka alkaloidi, kao što je arekolin, uzrokuju proliferaciju fibroblasta. Arome u pripravcima orašastih plodova areke, kao što su tanini, također mogu inhibirati aktivnost kolagenaze.
- Progresija bolesti povezana je sa zamjenom lako razgradivog kolagena tipa 1 otpornijim kolagenom tipa 3. Također postoji inhibicija fagocitoze kolagena.
- Patohistološki uzorci pokazat će određene značajke OSF, kao što su atrofija ili stanjivanje epitela i jukstaepitelna hijalinizacija i kolagen različite gustoće, zajedno s fibroziranom laminom proprijom i usidrenim vlakancima.
Epidemiologija
OSF se uglavnom javlja na indijskom potkontinentu i jugoistočnoj Aziji uključujući Indiju, Tajvan, Kinu, Bangladeš, Maleziju, Singapur, Tajland i Šri Lanku. Također je zabilježena u Južnoj Africi i Saudijskoj Arabiji. OSF se nalazi u azijskoj populaciji u SAD, Ujedinjenom Kraljevstvu i razvijenim zemljama te stoga ovo stanje predstavlja globalni zdravstveni teret. Broj globalnih slučajeva u 1996. procijenjen je na 2,5 milijuna. Prevalencija u Indiji iznosi čak 30%. Potrošnja areka orašastih plodova na globalnoj razini iznosi čak 5-20%. Simptomi OSF obično se razvijaju u 4. i 5. desetljeću života, ali zabilježeni su i slučajevi u bolesnika u dobi od jedanaest godina. Bolest iz nepoznatih razloga češće zahvaća žene.
Klinički izgled
- More (2012.) je klinički kategorizirao OSF u četiri stadija, uključujući eruptivnu, a zatim fibroznu fazu.
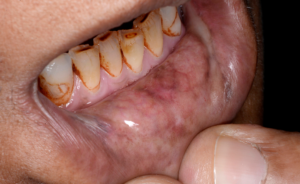
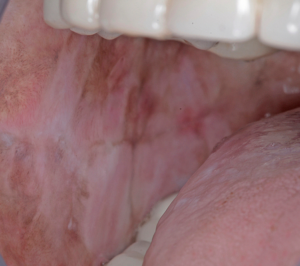
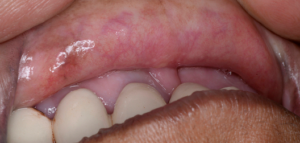
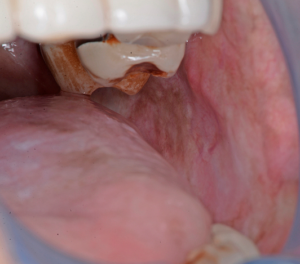
- Eruptivna faza može biti povezana sa stvaranjem vezikula, uz osjećaj pečenja i nelagode u usnoj šupljini. Tekstura usne sluznice počinje se mijenjati, gubi svoju gipkost. Blijedilo sluznice napreduje, a sluznica poprima blijedi izgled. Mogu se razviti petehije sluznice, melanotična pigmentacija sluznice, ulceracije sluznice i eritematozna područja.
- U drugom stadiju kada zacijele vezikule i ulkusi javlja se fibroza. Vertikalne i kružne palpabilne fibrozne trake u bukalnoj sluznici i/ili orofarinksu razvijaju se sa ili bez stomatitisa. Tanje trake mogu biti prisutne u ranijim fazama u usporedbi s ovim opipljivim vrpcama.
- U trećem stadiju, palpabilne fibrozne trake mogu biti prisutne u bilo kojem dijelu usne šupljine sa ili bez stomatitisa. Četvrti stadij obuhvaća sve navedeno s razvojem potencijalno zloćudnog poremećaja ili oralnog karcinoma pločastih stanica.
- Specifični nalazi koji se mogu naći od druge do četvrte faze uključuju trizmus, depigmentaciju gingive, atrofičnu uvulu i depapilaciju jezika. Promjene u estetici lica mogu se primijetiti i kod potonuća obraza što nije u korelaciji s dobi ili statusom uhranjenosti.
- U teškim slučajevima može doći do poremećaja govora i sluha. Prijavljeno je da OSF u kasnijim fazama ima značajan utjecaj na kvalitetu života.
- More je također opisao funkcionalnu fazu OSF-a na temelju interincizalnog otvaranja usta; Faza 1 (veća ili jednaka 35 mm), faza 2 (između 25 i 35 mm), faza 3 (15 i 25 mm) i faza 4 (manje od 15 mm).
- Paymaster je 1956. prvi put izvijestio o potencijalno zloćudnom potencijalu ovog stanja.
- Postoje značajne geografske varijacije u prijavljenim stopama zloćudne preobrazbe. Stopa je općenito viša u Indiji, u usporedbi s drugim zemljama.
- Moguće objašnjenje za to je način na koji se areka orašasti plodovi pripremaju s dodatnim aditivima. Tajvanske studije otkrile su da se duhanski proizvodi općenito ne koriste zajedno s proizvodima od orašastih plodova areka i to bi moglo objasniti nižu stopu zloćudne preobrazbe u ovoj populaciji.
- Procjenjuje se da je stopa zloćudne preobrazbe između 1 i 9%.
- Viša stopa zloćudne preobrazbe uočena je u onih s istodobnom oralnom leukoplakijom.
- Karcinomi usne šupljine koji potječu od OSF se navode i kao slabije i kao jače agresivni u usporedbi s oralnim karcinomom koji potječe od drugih lezija u usnoj šupljini.
Diferencijalna dijagnoza
U ranim fazama, OSF se može pogrešno dijagnosticirati. Bolesnicima koji se žale na osjećaj peckanja s atrofijom sluznice može se dijagnosticirati oralna dizestezija, s ili bez temeljnog pridonosnog čimbenika kao što je hematološki deficit ili anemija. Pažljivo uzimanje povijesti bolesti i ispitivanje rekreativnih navika je ključno. OSF se može pojaviti sa značajkama sličnim drugim oralnim potencijalno zloćudnim poremećajima, kao što je oralni lihen planus.
Sklerodermija je autoimuno stanje koje zahvaća kožu, unutarnje organe i krvne žile. Karakterizira ga difuzna skleroza kože i drugog vezivnog tkiva. Sklerodermija se može pojaviti s fibroznim trakama u oralnoj sluznici i progresivnim trizmusom. Pacijenti sa sklerodermijom također će imati ekstraoralne tegobe. Mikrovaskularna slika i testiranje na autoantitijela pomažu u postavljanju dijagnoze sklerodermije.
Amiloidoza je karakterizirana taloženjem amiloidnih proteina (fibrilarnog proteina) u tkivima. Sustavna amiloidoza može se manifestirati makroglosijom ili progresivnim trizmusom. Pažljivo uzimanje anamneze, analiza krvi i biopsija pomažu u postavljanju dijagnoze.
U kasnijim fazama, OSF se može manifestirati kao oralni karcinom pločastih stanica, leukoplakija i eritroplakija.
Dijagnoza
- Pažljivo ispitivanje rekreativnih navika snažno će uputiti na dijagnozu OSF. Budući da je OSF potencijalno zloćudno stanje, nužna je incizijska biopsija.
- Patohistološka analiza je od pomoći u kliničkom stupnjevanju bolesti, u kojoj su raspodjela i broj fibroblasta, kolagenih vlakana, prisutnost i broj upalnih stanica i krvnih žila u korelaciji sa stadijem bolesti.
- Trauma od postupka biopsije izaziva određeni stupanj fibroze što može doprinijeti pogoršanju trizmusa.
- Određeni biomarkeri, kao što je mRNA, mogu utjecati na stadij bolesti, a genetska analiza uzoraka može predvidjeti buduću zloćudnu preobrazbu.
- Hematoksilin i eozin su najčešće boje koje se koriste u dijagnozi OSF.
Liječenje
Bolesnike treba savjetovati o daljnjoj uporabi areka oraha za žvakanje i njegovoj ulozi u etiopatogenezi i riziku od zloćudne preobrazbe te ih treba poticati da prestanu s tom navikom. OSF nosi značajan globalni teret bolesti i primarna prevencija je ključni fokus vladine strategije u zemljama unutar indijskog potkontinenta. Pristupi poput zabrane proizvoda biljke areka i njihovih pripravaka, kao i edukacija o štetnim učincima žvakanja areka orašastih plodova pokazali su se korisnima u primarnoj prevenciji kako na individualnoj tako i na populacijskoj razini. OSF se često kasno javlja što uzrokuje dvojbe u vezi liječenja.
» Konzervativno liječenje
Konzervativno liječenje
- U umjerenim do teškim stadijima OSF, stupanj fibroze je ireverzibilan, a liječenje je prvenstveno simptomatsko.
- Konzervativno liječenje progresivnog smanjenja otvaranja usta uključuje fizikalnu terapiju. Savjetuju se razne vježbe usmjerene na istezanje tkiva i jačanje žvačnih mišića. Uređaji izrađeni po narudžbi također mogu biti korisni u smanjenju trizmusa. Bolesnike se potiče na masažu žvačnih mišića. Oralnu higijenu treba pojačati jer pacijenti s OSF pokazuju višu razinu oralnih bolesti kao što su parodontna bolest, zubni karijes i halitoza.
- Bolesnicima koji se žale na opću oralnu nelagodu može se propisati anestetik. U naprednijim stadijima OSF, intralezijske injekcije kortikosteroida bile su korisne u smanjenju trizmusa.
» View less
» Kirurško liječenje
Kirurško liječenje
- Kirurško liječenje može biti indicirano u teškim slučajevima trizmusa i ima za cilj poboljšati otvaranje usta te žvačno i oralno zdravlje.
- Kirurški pristup obično uključuje uklanjanje fibroziranog tkiva, a cilj njege nakon zahvata je održavanje mogućnosti otvaranja usta nakon uklanjanja tkiva i opuštanja mišića.
- Jednostavna ekscizija fibroznih traka pogoršava stanje, jer jatrogena trauma od kirurškog zahvata dovodi do naknadne fibroze.
- Kronični trizmus kao rezultat OSF može dovesti do fizioloških promjena u tetivi temporalnog mišića, a postupci presađivanja kože mogu pomoći da se to riješi, na primjer presađivanje kože podijeljene debljine nakon bilateralne miotomije temporalisa ili koronoidektomije. To su opsežni kirurški zahvati i ne smiju se poduzeti olako, ali mogu ublažiti simptome trizmusa.
- Može se razmotriti i miotomija drugih žvačnih mišića.
» View less
Sažetak
OSF je kronično, progresivno stanje koje rezultira fibrozom sluznice orofarinksa i, povremeno, gornjeg jednjaka, kao rezultat fizioloških promjena uzrokovanih žvakanjem orašastih plodova areke. Areka orašasti plodovi i njegovi metaboliti su kancerogeni, a različiti pripravci orašastih plodova areka uključuju i druge karcinogene. Stopa zloćudne preobrazbe varira geografski i kreće se od 1-9%. Brzina zloćudne preobrazbe ovisi o dozi i korelira s trajanjem i intenzitetom navike žvakanja orašastih plodova areke te kada se koristi u kombinaciji s konzumiranjem alkohola i duhana. Ne postoji univerzalno prihvaćen protokol liječenja.
Globalno gledano, znanje o stanju među općom populacijom i zdravstvenim radnicima je nisko. To može doprinijeti kasnom postavljanju dijagnoze ovih bolesnika. Svi zdravstveni radnici imaju ulogu u primarnoj prevenciji i prepoznavanju bolesti.
Literatura
J.D. Langdon, in Oral and Maxillofacial Surgery (Second Edition), 2007
Brad W. Neville DDS, … Angela C. Chi DMD, in Color Atlas of Oral and Maxillofacial Diseases, 2019
Raman Bedi, Crispian Scully, in Manson’s Tropical Infectious Diseases (23.izdanje), 2014
More C, Gupta S, Joshi J, Varma S. Classification system of Oral submucous fibrosis. J Indian Acad Oral Med Radiol. 2012;24(1):24–9
Ali, F. M., Patil, A., Patil, K. and Prasant, M. C. (2014) ‘Oral submucous fibrosis and its dermatological relation’, Indian Dermatol Online J, 5(3), pp. 260-5.
Angadi, P. V. and Rao, S. S. (2011) ‘Areca nut in pathogenesis of oral submucous fibrosis: revisited’, Oral Maxillofac Surg, 15(1), pp. 1-9.
Arakeri, G., Patil, S. G., Aljabab, A. S., Lin, K. C., Merkx, M. A. W., Gao, S. and Brennan, P. A. (2017a) ‘Oral submucous fibrosis: An update on pathophysiology of malignant transformation’, J Oral Pathol Med, 46(6), pp. 413-417.
Arakeri, G., Rai, K. K., Boraks, G., Patil, S. G., Aljabab, A. S., Merkx, M. A. W., Carrozzo, M. and Brennan, P. A. (2017b) ‘Current protocols in the management of oral submucous fibrosis: An update’, J Oral Pathol Med, 46(6), pp. 418-423.
Arakeri, G., Rai, K. K., Hunasgi, S., Merkx, M. A. W., Gao, S. and Brennan, P. A. (2017c) ‘Oral submucous fibrosis: An update on current theories of pathogenesis’, J Oral Pathol Med, 46(6), pp. 406-412.
Cox, S. C. and Walker, D. M. (1996) ‘Oral submucous fibrosis. A review’, Aust Dent J, 41(5), pp. 294-9.
Garg, A., Chaturvedi, P. and Gupta, P. C. (2014) ‘A review of the systemic adverse effects of areca nut or betel nut’, Indian J Med Paediatr Oncol, 35(1), pp. 3-9.
Gupta, P. C. and Warnakulasuriya, S. (2002) ‘Global epidemiology of areca nut usage’, Addict Biol, 7(1), pp. 77-83.
Kim, D. H., Lee, J., Lee, M. H., Kim, S. W. and Hwang, S. H. (2020) ‘Efficacy of chemiluminescence in the diagnosis and screening of oral cancer and precancer: a systematic review and meta-analysis’, Braz J Otorhinolaryngol.
Murti, P. R., Bhonsle, R. B., Pindborg, J. J., Daftary, D. K., Gupta, P. C. and Mehta, F. S. (1985) ‘Malignant transformation rate in oral submucous fibrosis over a 17-year period’, Community Dent Oral Epidemiol, 13(6), pp. 340-1.
Pandya, S., Chaudhary, A. K., Singh, M. and Mehrotra, R. (2009) ‘Correlation of histopathological diagnosis with habits and clinical findings in oral submucous fibrosis’, Head Neck Oncol, 1, pp. 10.
Passi, D., Bhanot, P., Kacker, D., Chahal, D., Atri, M. and Panwar, Y. (2017) ‘Oral submucous fibrosis: Newer proposed classification with critical updates in pathogenesis and management strategies’, Natl J Maxillofac Surg, 8(2), pp. 89-94.
PAYMASTER, J. C. (1956) ‘Cancer of the buccal mucosa; a clinical study of 650 cases in Indian patients’, Cancer, 9(3), pp. 431-5.
Pindborg, J. J. and Sirsat, S. M. (1966) ‘Oral submucous fibrosis’, Oral Surg Oral Med Oral Pathol, 22(6), pp. 764-79.
Rai, A., Ahmad, T., Parveen, S., Faizan, M. I. and Ali, S. (2020) ‘Expression of transforming growth factor beta in oral submucous fibrosis’, J Oral Biol Craniofac Res, 10(2), pp. 166-170.
Rai, S., Rattan, V., Gupta, A. and Kumar, P. (2018) ‘Conservative management of Oral Submucous Fibrosis in early and intermediate stage’, J Oral Biol Craniofac Res, 8(2), pp. 86-88.
Rajendran, R. (1994) ‘Oral submucous fibrosis: etiology, pathogenesis, and future research’, Bull World Health Organ, 72(6), pp. 985-96.
Rao, N. R., Villa, A., More, C. B., Jayasinghe, R. D., Kerr, A. R. and Johnson, N. W. (2020) ‘Oral submucous fibrosis: a contemporary narrative review with a proposed inter-professional approach for an early diagnosis and clinical management’, J Otolaryngol Head Neck Surg, 49(1), pp. 3.
Shih, Y. H., Wang, T. H., Shieh, T. M. and Tseng, Y. H. (2019) ‘Oral Submucous Fibrosis: A Review on Etiopathogenesis, Diagnosis, and Therapy’, Int J Mol Sci, 20(12).
Silva, W. P., Wastner, B. F., Bohn, J. C., Jung, J. E., Schussel, J. L. and Sassi, L. M. (2015) ‘Unusual presentation of oral amyloidosis’, Contemp Clin Dent, 6(Suppl 1), pp. S282-4.
Yoithapprabhunath, T. R., Maheswaran, T., Dineshshankar, J., Anusushanth, A., Sindhuja, P. and Sitra, G. (2013) ‘Pathogenesis and therapeutic intervention of oral submucous fibrosis’, J Pharm Bioallied Sci, 5(Suppl 1), pp. S85-8.







