Leucoplasia
Ao longo dos últimos 40 anos, várias definições têm sido sugeridas para a Leucoplasia Oral (LO), sendo um processo em constante evolução (Tabela 1). A definição mais recente e amplamente aceite foi proposta pelo grupo de trabalho do Collaborating Center for Oral Cancer/Precancer da OMS em 2007 e reconfirmada em 2020. A leucoplasia é definida como “uma placa predominantemente branca de risco questionável que exclui (outras) doenças ou alterações conhecidas que não apresentam aumento de risco de se transformar em cancro”.
O termo leucoplasia é utilizado após exclusão de qualquer outra condição da mucosa oral que possa apresentar-se como uma lesão branca (por exemplo, queratose friccional, líquen plano, nevus branco esponjoso, leucoplasia pilosa, etc.). Por definição, a leucoplasia é uma entidade clínica, de diagnóstico por exclusão e não possui um componente histopatológico específico.
Epidemiologia e Fatores de Risco para o Desenvolvimento de Leucoplasia Oral
Epidemiologia:
- Normalmente diagnosticada em pacientes de meia-idade e idosos.
- Maior incidência em indivíduos do sexo masculino.
- A LO é seis vezes mais comum em fumadores do que em não-fumadores.
- A sua prevalência varia significativamente em função da área geográfica devido a diferentes fatores de risco, como o hábito de mascar bétele no Sudoeste Asiático.
Fatores de Risco:
- A LO está associada a vários fatores de risco, semelhantes aos observados no cancro oral, como os hábitos tabágicos (cigarros normais ou cigarros sem fumo), consumo excessivo de álcool, mascar bétele (sobretudo em países do Sudoeste Asiático) e, especialmente em lesões que envolvem o lábio e à exposição à luz ultravioleta (UV).
- O consumo de álcool é um fator de risco independente. Foi estabelecido que esses fatores podem ter um papel etiológico no desenvolvimento de LO em mais de 75% dos indivíduos afetados.
Manifestações Clínicas
- A LO pode surgir em qualquer parte da cavidade oral e apresentar-se como lesão única podendo, no entanto, ser multifocal. Contudo, nas populações industrializadas ocidentais, os locais mais afetados são o bordo lateral da língua e o pavimento da boca.
- Em populações asiáticas, devido ao consumo frequente de bétele, as mucosas oral e labial são frequentemente afetadas.
- Clinicamente, a leucoplasia tem um leque de possíveis manifestações variáveis na aparência (branco, vermelho e branco e vermelho misto, placa granular, atrófica) textura (lisa, ondulada, granular, verrucosa, macia, firme ou dura), tamanho e forma.
- A extensão clínica da leucoplasia oral pode variar em tamanho, desde uma lesão relativamente pequena e bem circunscrita até uma lesão extensa, envolvendo uma grande área da mucosa oral.
A leucoplasia pode ser subclassificada clinicamente em dois tipos: homogénea e não-homogénea. Figuras 1 e 2.
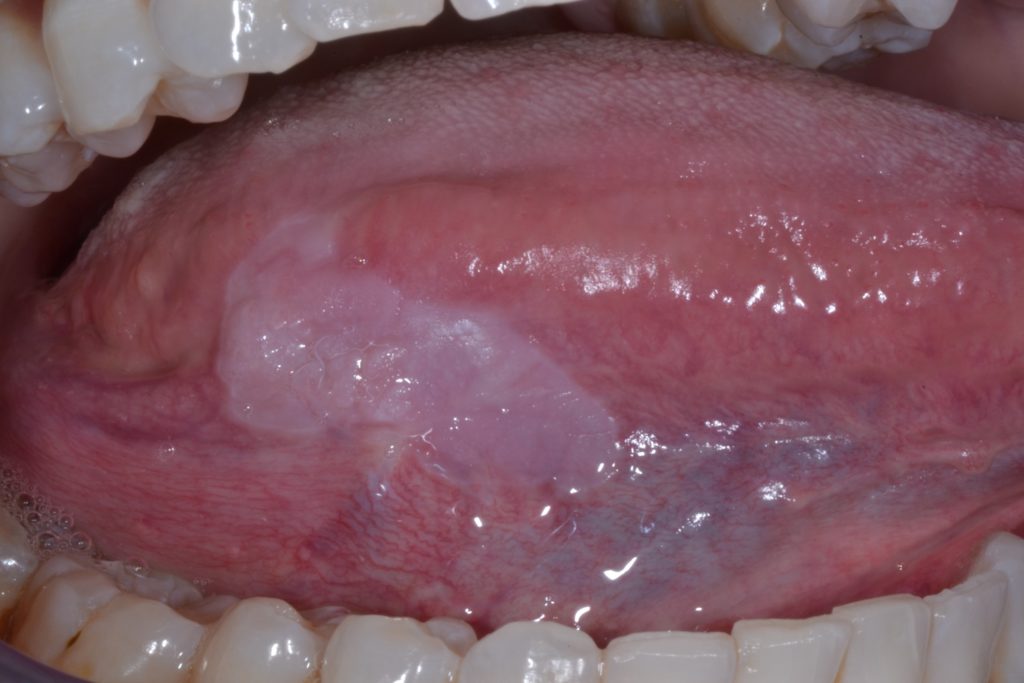
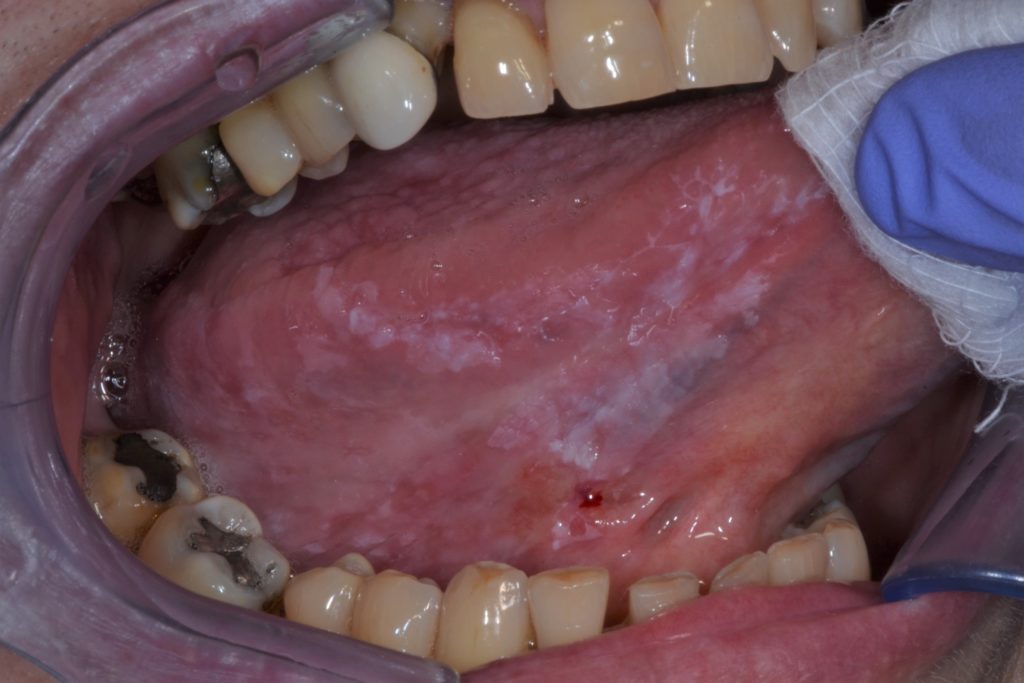
Esta distinção é puramente clínica, baseada em manifestações distintas como superfície, cor e textura: leucoplasia homogénea e leucoplasia não-homogénea (Tabela 2).
| Leucoplasia Oral | |
| Leucoplasia homogénea | Leucoplasia não-homogénea |
| Placa/mancha branca plana e fina uniforme com margens bem definidas, superfície lisa associada a fissuras rasas. Não pode ser removido através de raspagem. | Pontilhada: Coloração branca e vermelha, simultânea Nodular: pequenos crescimentos polipoides e excrescências arredondadas Verrucosa ou exofítica : superfície de aparência enrugada. Não pode ser removida através de raspagem. |
Tabela 2: Classificação da leucoplasia oral com base nas distintas manifestações clínicas.
Leucoplasia Homogénea:
- Caracterizada por uma placa/mancha branca, plana e fina, uniforme, com margens bem definidas e superfície lisa que pode estar associada a fissuras rasas da queratina superficial. Ilustrado em detalhe na Figura 3
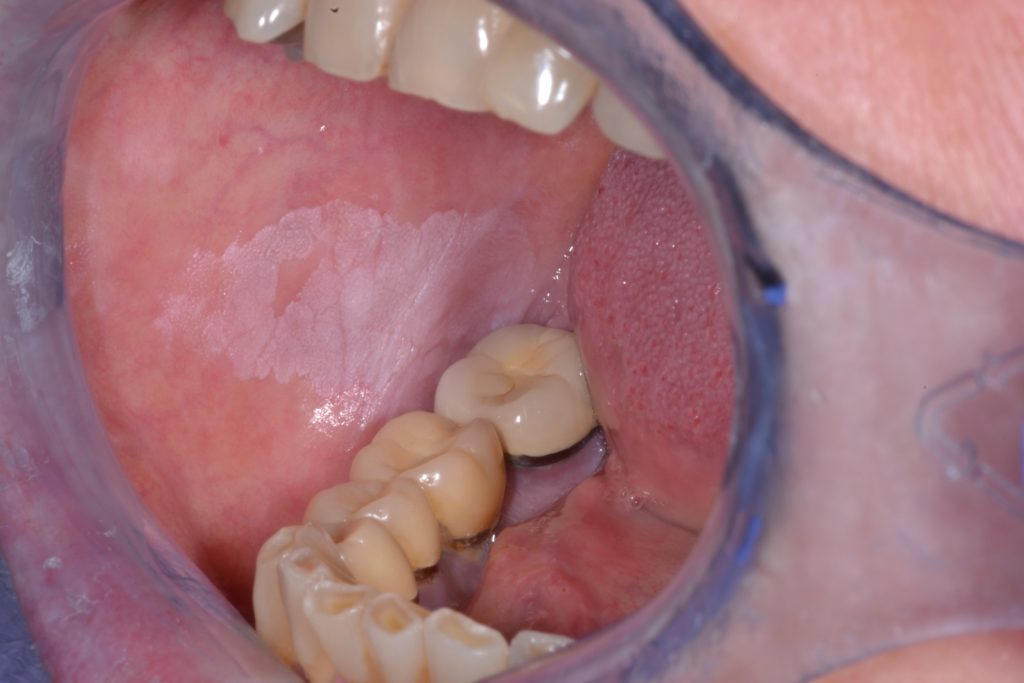
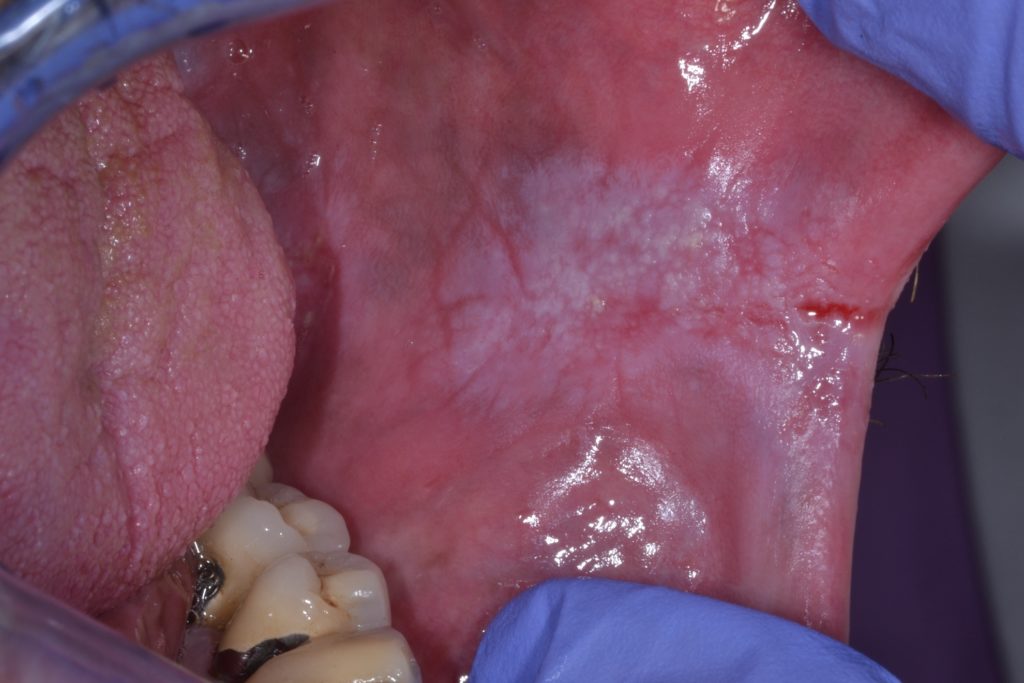
Leucoplasia Não-homogénea:
- Caracterizada por textura irregular, que pode incluir ulceração superficial e margens mal definidas. A leucoplasia não-homogénea pode estar associada a diferentes manifestações clínicas utilizadas na sua descrição: Ilustrado em detalhe nas Figuras 4 e 5.
- Pontilhada: coloração branca e vermelha simultaneamente, sendo predominante a coloração branca (também definida como eritroleucoplasia)
- Nodular: pequenos crescimentos polipoides, excrescências arredondadas, vermelhas ou brancas
- Verrucosa ou exofítica: superfície de aparência enrugada ou corrugada
- As formas de leucoplasia são geralmente assintomáticas e são normalmente identificadas durante o exame de rotina.
- A leucoplasia homogénea é geralmente assintomática.
- Os sintomas são raros e, se existentes, estão geralmente associados às formas não-homogéneas, que poderão apresentar ulceração superficial.
- Os sintomas relatados com mais frequência são o desconforto, a sensação de formigueiro e sensibilidade ao toque aquando do consumo de bebidas quentes ou alimentos condimentados.
Risco de Evolução para Cancro
Carcinoma de Células Escamosas Oral:
- O Carcinoma de Células Escamosas é a forma de neoplasia mais comum que afeta a cavidade oral.
- Este tipo de cancro geralmente afeta homens com mais de 60 anos; no entanto, recentemente a prevalência aumentou naqueles com menos de 40 anos.
- Pode apresentar-se como uma úlcera que não cicatriza, massa crescente com superfície irregular e lesões vermelhas ou brancas do epitélio oral.
Leucoplasia:
- As leucoplasias são classificadas como alterações orais potencialmente malignas que predispõem os indivíduos afetados a um risco aumentado de desenvolvimento de Carcinoma de Células Escamosas Oral.
- A LO apresenta percentagens variáveis de progressão para Carcinoma de Células Escamosas, com taxas entre os 0% a 36,4%. A taxa anual de transformação varia de 0,3% a 6,9%, conforme relatado por uma revisão recente de estudos observacionais.
- Os fatores de risco estatisticamente relevantes na evolução para cancro em indivíduos diagnosticados com LO estão enumerados na tabela 4.
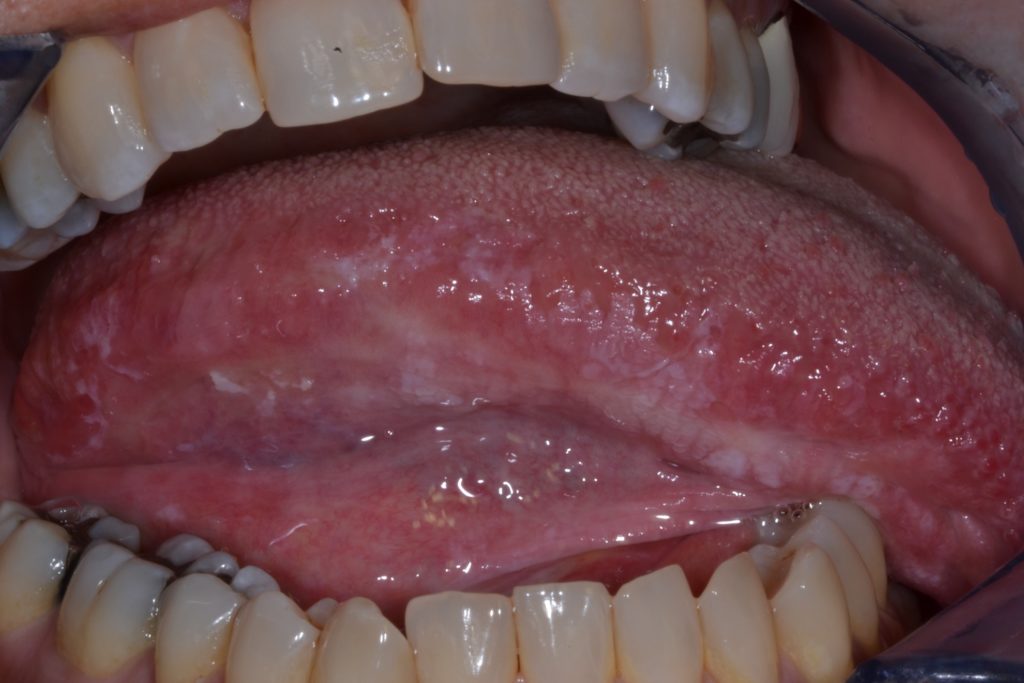
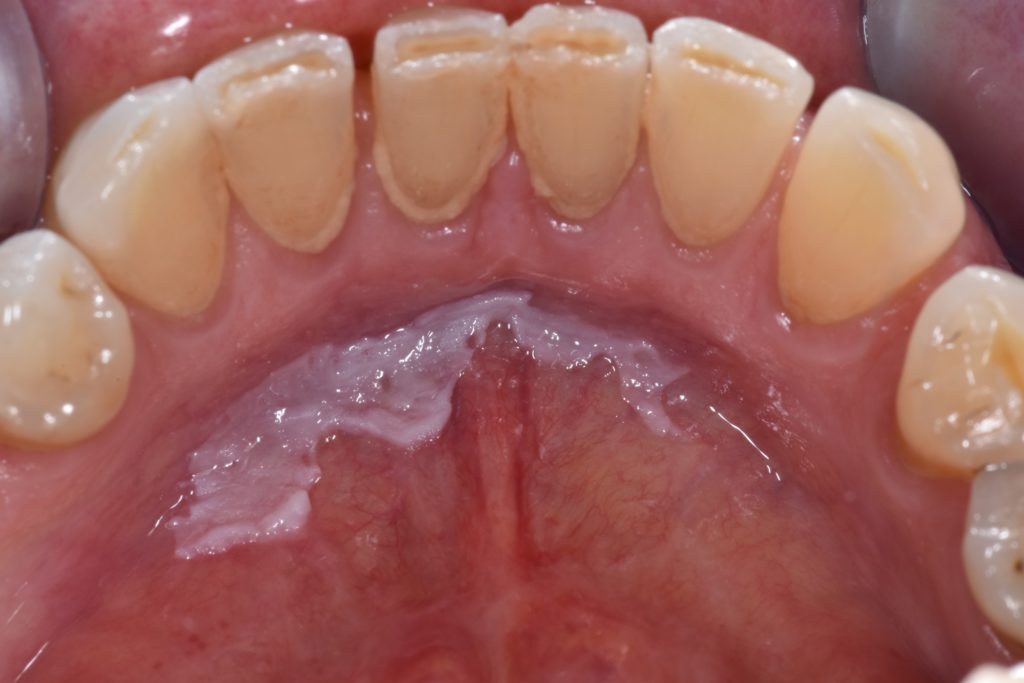
- A Figura 6 ilustra leucoplasia do pavimento da boca (mucosa por baixo da língua), considerada um local de alto risco devido à acumulação de carcinógenos.
| Leucoplasia oral – Fator de risco de transformação maligna |
| Aspeto não-homogéneo |
| Género feminino |
| Leucoplasia de longa duração |
| Leucoplasia idiopática (não causada por tabagismo/ingestão de álcool/mascar) |
| Localização: lateral da língua e/ou pavimento da boca (mucosa por baixo da língua) |
| Tamanho > 200 mm2 |
| Presença de displasia epitelial |
| Presença de Candida albicans (candidose hiperplástica crónica ou leucoplasia por candida) [35] |
Tabela 3. Fatores de risco de transformação maligna na leucoplasia oral
Transformação da Leucoplasia em Carcinoma de Células Escamosas:
- Leucoplasias com características clínicas, histológicas ou moleculares diferentes podem apresentar riscos distintos de se transformarem em Carcinoma de Células Escamosas da Cavidade Oral.
- As leucoplasias não-homogéneas apresentam um risco maior de desenvolvimento para carcinoma de células escamosas quando comparadas a leucoplasias homogéneas – existe um risco de aproximadamente 7 vezes maior de transformação maligna nos casos de leucoplasia não homogénea, enquanto que nos casos de leucoplasia homogénea o risco da transformação maligna é 5 vezes maior, quando o tamanho da lesão é superior a 200mm2
- Nas populações ocidentais, as mulheres idosas com leucoplasia idiopática de longa data, sem fatores de risco, paradoxalmente, têm um risco aumentado de progressão para cancro oral – provavelmente devido a fatores de risco endógenos e não ambientais.
- A vermelhidão numa lesão de LO (não-homogénea) indica uma potencial colonização por Candida e um risco aumentado de ocorrência de displasia e/ou malignidade.
- O grau de displasia é aceite como um forte indicador de futura transformação maligna da LO, e continua a ser a melhor ajuda para avaliar o risco de evolução para cancro oral.
- A leucoplasia não-homogénea exibe, frequentemente, displasia grave ou Carcinoma de Células Escamosas Oral superficialmente invasivo no momento da biópsia inicial.
- O risco de evolução para cancro está intimamente relacionado com o tipo de lesão e com o grau de displasia.
Diagnóstico da Leucoplasia
É obrigatório um exame intraoral sistemático, com palpação dos nódulos linfáticos cervicais [5]. Conforme descrito acima, o termo leucoplasia é um diagnóstico clínico após exclusão de outras lesões brancas ou brancas/vermelhas clinicamente reconhecíveis. Os seguintes critérios devem ser considerados ao fazer um diagnóstico clínico de leucoplasia oral:
- Mancha/placa branca que não pode ser removida
- A leucoplasia homogénea geralmente apresenta bordas bem demarcadas
- A leucoplasia não-homogénea apresenta frequentemente componentes vermelhos ou nodulares e bordas mais difusas
- Não existe qualquer evidência de irritação traumática crónica relacionada
- Não é reversível com a eliminação das causas traumáticas aparentes
- Não desaparece ao retarir o tecido
- Exclusão de outras lesões de cor branca/vermelha
Carrard e van der Waal propuseram recentemente uma lista de parâmetros que podem ser relevantes no estabelecimento de um diagnóstico clínico de leucoplasia oral. Identificam-se alguns na tabela (Tab. 4)
| Característica | Papel e relevância durante o diagnóstico clínico da leucoplasia oral |
| Idade | A LO raramente ocorre nas primeiras duas décadas de vida. |
| Historial médico | Relevante para o diagnóstico de várias doenças semelhantes à leucoplasia, como manifestações orais de genodermatose, sífilis e infeção por HIV. |
| Hábitos tabágicos de qualquer tipo | Mais comum em fumadores |
| Sintomatologia | A maioria das LO são assintomáticas, mas pode ocorrer dor ou prurido. |
| Início da doença | A LO tem um desenvolvimento lento, no decorrer de vários meses ou anos |
| Desenvolvimento da doença | Apresenta um percurso clínico estável |
| Morfologia | |
| Tamanho | O tamanho não é relevante no diagnóstico clínico de LO. |
| Cor | A cor pode variar entre um branco homogéneo e uma apresentação branco/vermelha. |
| Textura | A textura pode variar de lisa, enrugada a verrucosa. A ulceração pode ser indicativa de malignidade. |
| Endurecimento | A palpação é uma ferramenta de diagnóstico muito importante, sendo que o endurecimento pode ser um indicador de natureza potencialmente maligna. |
Tabela 4: Listagem de algumas características, modificadas de Carrard e van der Waal, que podem ser úteis no diagnóstico clínico e na avaliação da leucoplasia
- O procedimento gold standard para confirmar o diagnóstico clínico de leucoplasia oral é realizar uma biópsia incisional representativa da lesão da mancha branca e enviar o tecido para análise histopatológica.
- A realização de uma biópsia é obrigatória para confirmar ou descartar o diagnóstico de LO. A biópsia e a análise histopatológica subsequente permitem excluir outras patalogias que podem apresentar-se como uma placa branca, como a colonização de Candida no epitélio.
- A biópsia é necessária para excluir o diagnóstico de Carcinoma de Células Escamosas Oral (CCEO) e para avaliar a presença e o grau de displasia epitelial.
- Os resultados da análise histopatológica associados à leucoplasia oral podem variar desde simples hiperplasia epitelial com hiperparaqueratose ou hiper(orto)queratose, presença ou ausência de displasia epitelial e o seu grau.
Embora tenha já sido proposta uma classificação binária para a displasia oral (baixo e alto grau), o sistema de três graus (leve, moderado ou grave) é ainda amplamente utilizado na prática clínica em todo o mundo.
Diagnóstico Diferencial de Manchas Brancas
Durante o exame clínico de uma lesão de cor branca, é importante avaliar possíveis causas traumáticas locais e, se identificada, a mancha branca deve ser designada como queratose friccional. A queratose friccional não é considerada uma Alteração Oral Potencialmente Maligna e a remoção da fonte de atrito suspeita deverá eliminar a lesão.
Na tabela seguinte encontra-se uma lista detalhada das lesões e alterações de cor branca mais relevantes que devem ser excluídos antes de estabelecer um diagnóstico clínico de leucoplasia oral (Tabela 5).
| Diagnóstico diferencial com LO | Descrição |
| Nevus branco esponjoso | Detetado no início da vida e por vezes com histórico familiar. Localização bilateral, normalmente extensiva na boca, sendo que a mucosa genital também pode ser afetada. |
| Linha alba | De diagnóstico clínico, é quase sempre bilateral e ocorre ao longo da linha de oclusão. |
| Leucoedema | Diagnóstico clínico com aspeto de véu, bilateral na mucosa oral, e desaparece esticando os tecidos. Predileção entre alguns grupos raciais: pessoas de pele escura, no período da meia-idade. |
| Grânulos de Fordyce | Manchas/pápulas de 1-2 mm de diâmetro, distintamente demarcadas do normal revestimento da mucosa. Apresentam-se como protuberâncias, de forma circular, de cor amarelada/branca. |
| Morsicatio buccarum | Condição caracterizada por irritação crónica ou lesão da mucosa oral, comissuras ou bochechas, causada por mastigação ou mordida habitual e repetitiva. Observam-se flocos irregulares amarelo-esbranquiçados com linhas irregulares, frequentemente bilaterais. |
| Queratose friccional* | Historial clínico positivo de fricção ou outro trauma mecânico. Normalmente é revertida após remoção do fator etiológico. |
| Lesões queratóticas | Incluem: queratose dos fumadores “reversos”, queratose do rebordo alveolar (ARK), queratose friccional, queratose associada à sanguinaria, queratose da bolsa de tabaco e queratose de origem desconhecida (KUS). A queratose do fumador “reverso” e a queratose da bolsa de tabaco têm potencial maligno. |
| Lesão química | Historial de exposição prolongada a um agente químico (por exemplo, aspirina) ou a um agente cáustico (por exemplo, hipoclorito de sódio). A lesão provoca dor, mas é de resolução geralmente rápida |
| Estomatite nicotínica (palato do fumador) | Palato branco-acinzentado com manchas vermelhas relacionadas com a inflamação de glândulas salivares menores. Normalmente, existe diagnóstico clínico associado ao histórico de tabagismo. |
| Estomatite urémica | Placas brancas, bem demarcadas, aderentes de exsudato fibrinoso com algumas células epiteliais descamadas. O diagnóstico está associado à história positiva para doença renal. |
| Quilite actínica | O lábio inferior é a área mais afetada, com lesão branca. A manifestação clínica típica pode variar e podem ocorrer alterações semelhantes à leucoplasia. |
| Líquen Plano Oral (LPO) | Nas suas apresentações típicas, podem ver-se pápulas brancas juntas a linhas que formam uma aparência reticular na superfície de uma mucosa com inflamação. Apresentação bilateral regular. O LPO pode ainda apresentar-se como gengivite descamativa. Podem verificar-se vários subtipos clínicos de líquen plano: Reticular: linhas brancas tipo renda Linear, anelar, papular: várias apresentações como linhas, anéis ou pontos brancos Em Placa: placas brancas com margens estriadas Atrófica e ulcerativa: vermelha e visivelmente ulcerada Bulhosa: o LPO vesicular em placa pode ser difícil de diagnosticar da leucoplasia oral. O LPO está incluído no grupo de alterações orais potencialmente malignas [1] |
| Lesão liquenoide por contacto direto | Causada pelo contato direto prolongado da mucosa oral com amálgama ou outro tipo de restauração. A lesão deve desaparecer em um período escolhido arbitrariamente de 2 a 3 meses após a remoção da restauração. |
| Candidíase pseudomembranosa aguda | Infeção geralmente generalizada da mucosa oral e, às vezes, da orofaringe. A membrana branca pode ser raspada, por vezes revelando uma pegada eritematosa/crua. Associado a causas subjacentes locais (por exemplo, esteroides em spray inalados) ou sistémicas (por exemplo, imunodeficiência). |
| Candidíase hiperplásica crónica (leucoplasia por Candida) | Uma mancha branca ou branca e vermelha aderente causada por uma infeção fúngica crónica, geralmente Candida albicans. Localizado principalmente na área retrocomissural, muitas vezes bilateral. O tratamento antifúngico é utilizado para avaliar a regressão das lesões e confirmar o diagnóstico. |
| Leucoplasia pilosa | Queratose com estrias verticais, causada por infeção oportunista pelo vírus Epstein Bar, que muitas vezes é bilateral e mais comum nos bordos laterais da língua. Historial de imunossupressão por HIV ou fármacos (por exemplo, após transplante de órgãos/esteroides de longo prazo). |
| Sífilis secundária | O diagnóstico deve avaliar o historial clínico e demonstrar positividade sorológica para Treponema Pallidum. A manifestação clínica pode ser variada: múltiplas “manchas mucosas” liquenoides esbranquiçadas e alterações semelhantes a leucoplasia da mucosa oral e múltiplas lesões vermelhas no dorso da língua e palato. |
| Papiloma e lesões relacionadas com o HPV (por exemplo, condiloma acuminado, hiperplasia epitelial multifocal, verruga vulgar). | O diagnóstico é baseado na aparência clínica das lesões e no historial clínico. Geralmente é útil realizar uma biópsia associada à tipificação do HPV. |
Tabela 5: Lista detalhada das principais lesões brancas, condições ou doenças que devem ser excluídas antes de estabelecer um diagnóstico clínico de leucoplasia oral (modificado por [1,9])
Tratamento e Prevenção
O objetivo principal no tratamento da leucoplasia oral deve ser monitorizar e prevenir o aparecimento do cancro oral. Numa tentativa conjunta de reduzir as hipóteses de desenvolvimento de cancro, vários tratamentos e protocolos de controlo foram propostos. As principais abordagens na gestão da LO podem ser divididas em três grupos:
- Plano terapêutico (tópico ou sistémico)
- Observação clínica (“esperar e ver”); sem intervenção, assente numa vigilância clínica e histológica rigorosas).
- Intervenção cirúrgica: realizada através de diferentes técnicas (bisturi, cirurgia a laser (excisão e vaporização, criocirurgia))
Não há consenso sobre a abordagem mais adequada para a LO.
Tratamento Médico
Nenhum dos tratamentos médicos e complementares estudados (vitamina A, betacaroteno, bleomicina) se mostrou eficaz na prevenção do aparecimento de cancro em indivíduos com LO. Vários estudos quimopreventivos também evidenciaram uma considerável toxicidade dos fármacos utilizados. O tratamento médico da leucoplasia pode ser eficaz na redução ou resolução da leucoplasia oral a curto prazo, mas tem sido associado a um alto risco de recidiva.
Abordagem “Esperar e Ver”
Outra abordagem pode passar por manter um caso de leucoplasia sob rigorosa vigilância clínica e histológica, com visitas clínicas frequentes (examinação) e biópsias com o objetivo de detetar a transformação maligna o mais precocemente possível, proporcionando assim o melhor prognóstico. Esta abordagem é baseada no conceito de “cancerização em campo”, proposto por Slaughter em 1957. Segundo o mesmo, se um carcinógeno desenvolveu para uma alteração pré-maligna ou maligna clinicamente detetável numa parte da cavidade oral, há uma taxa de risco igual para incidência noutras partes da cavidade oral. A LO pode ser considerada um indicador de risco para toda a mucosa oral e não apenas para uma área localizada específica. Um ECR recente avaliou a eficácia da excisão cirúrgica, em comparação com o tratamento padrão na prevenção de Carcinoma de Células Escamosas Oral em 260 indivíduos com LO não displásica.
Cirurgia
Existe um único Ensaio Aleatório Controlado (RCT) que comparou o efeito da excisão cirúrgica contra nenhum tratamento ou placebo. Apesar disso, os tratamentos cirúrgicos são, para a maioria dos clínicos, o tratamento de escolha para a leucoplasia oral. A excisão cirúrgica é frequente e algumas evidências sugerem que reduz o risco de transformação maligna quando comparado à monitorização ativa. Apenas dados de estudos observacionais compararam taxas de incidência de cancro em pessoas que fizeram ou não tratamento cirúrgico para leucoplasias orais com diferenças nos critérios diagnósticos e de inclusão, intervalos de acompanhamento, características dos participantes e técnicas cirúrgicas utilizadas. Esses estudos mostraram resultados altamente variáveis e conflitantes nas suas conclusões.
A intervenção cirúrgica com excisão com bisturi frio e/ou laser de CO2 é geralmente realizada em casos de leucoplasia não-homogénea ou eritroplasia, associada a displasia moderada a grave.
Conclusão
A cirurgia continua a ser a opção de tratamento preferida pela maioria; no entanto, a eficácia da cirurgia em comparação com o acompanhamento clínico regular não foi avaliada em RCTs para prevenção do desenvolvimento de cancro. Até ao momento, apenas um RCT comparou tratamentos cirúrgicos com a inexistência de tratamento. Na ausência de indicadores RCT robustos, a prática clínica mantém-se variável.
Referências e Leitura Recomendada
Warnakulasuriya, S.; Kujan, O.; Aguirre‐Urizar, J.M.; Bagan, J. V.; González‐Moles, M.Á.; Kerr, A.R.; Lodi, G.; Mello, F.W.; Monteiro, L.; Ogden, G.R.; et al. Oral potentially malignant disorders: A consensus report from an international seminar on nomenclature and classification, convened by the WHO Collaborating Centre for Oral Cancer. Oral Dis. 2020, odi.13704, doi:10.1111/odi.13704.
van der Waal, I. Oral leukoplakia, the ongoing discussion on definition and terminology. Med. Oral Patol. Oral Cir. Bucal 2015, 20, e685–e692, doi:10.4317/medoral.21007.
Lodi, G.; Franchini, R.; Warnakulasuriya, S.; Varoni, E.M.; Sardella, A.; Kerr, A.R.; Carrassi, A.; Macdonald, L.C.I.; Worthington, H. V. Interventions for treating oral leukoplakia to prevent oral cancer. Cochrane Database Syst. Rev. 2016.
Amagasa, T.; Yamashiro, M.; Uzawa, N. Oral premalignant lesions: From a clinical perspective. Int. J. Clin. Oncol. 2011, 16, 5–14, doi:10.1007/s10147-010-0157-3.
Warnakulasuriya, S. Clinical features and presentation of oral potentially malignant disorders. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018, 125, 582–590.
Staines, K.; Rogers, H. Oral leukoplakia and proliferative verrucous leukoplakia: A review for dental
Speight, P.M.; Khurram, S.A.; Kujan, O. Oral potentially malignant disorders: risk of progression to malignancy. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018.
Napier, S.S.; Speight, P.M. Natural history of potentially malignant oral lesions and conditions: An overview of the literature. J. Oral Pathol. Med. 2008, 37, 1–10.
Carrard, V.; van der Waal, I. A Clinical Diagnosis of Oral Leukoplakia . Med Oral Patol Oral Cir Bucal 2018.
Sundberg, J.; Korytowska, M.; Holmberg, E.; Bratel, J.; Wallström, M.; Kjellström, E.; Blomgren, J.; Kovács, A.; Öhman, J.; Sand, L.; et al. Recurrence rates after surgical removal of oral leukoplakia-A prospective longitudinal multicentre study. PLoS One 2019, 14, doi:10.1371/journal.pone.0225682.
Petti, S. Pooled estimate of world leukoplakia prevalence: A systematic review. Oral Oncol. 2003,
Villa, A.; Sonis, S. Oral leukoplakia remains a challenging condition. Oral Dis. 2018, 24, 179–183, doi:10.1111/odi.12781.
Mello, F.W.; Miguel, A.F.P.; Dutra, K.L.; Porporatti, A.L.; Warnakulasuriya, S.; Guerra, E.N.S.; Rivero, E.R.C. Prevalence of oral potentially malignant disorders: A systematic review and
Jayasooriya, P.R.; Dayaratne, K.; Dissanayake, U.B.; Warnakulasuriya, S. Malignant transformation of oral leukoplakia: a follow-up study. Clin. Oral Investig. 2020, doi:10.1007/s00784-020-03322-4.
Warnakulasuriya, S. Oral potentially malignant disorders: A comprehensive review on clinical aspects and management. Oral Oncol. 2020, 102, doi:10.1016/j.oraloncology.2019.104550.
Arduino, P.; Bagan, J.; El-Naggar, A.; Carrozzo, M. Urban legends series: Oral leukoplakia. Oral Dis. 2013, 19, 642–659.
Villa, A.; Celentano, A.; Glurich, I.; Borgnakke, W.S.; Jensen, S.B.; Peterson, D.E.; Delli, K.; Ojeda, D.; Vissink, A.; Farah, C.S. World Workshop on Oral Medicine VII: Prognostic biomarkers in oral leukoplakia: A systematic review of longitudinal studies. Oral Dis. 2019, 25, 64–78.
Villa, A.; Woo, S. Bin Leukoplakia—A Diagnostic and Management Algorithm. J. Oral Maxillofac. Surg. 2017, 75, 723–734.
Syrjänen, S.; Lodi, G.; von Bültzingslöwen, I.; Aliko, A.; Arduino, P.; Campisi, G.; Challacombe, S.; Ficarra, G.; Flaitz, C.; Zhou, H.; et al. Human papillomaviruses in oral carcinoma and oral potentially malignant disorders: A systematic review. Oral Dis. 2011, 17, 58–72, doi:10.1111/j.1601-0825.2011.01792.x.
Varoni, E.M.; Lombardi, N.; Franchini, R.; D’Amore, F.; Noviello, V.; Cassani, B.; Moneghini, L.; Sardella, A.; Lodi, G. Oral Human Papillomavirus (HPV) and sexual behaviors in a young cohort of oral cancer survivors. Oral Dis. 2020, odi.13622, doi:10.1111/odi.13622.
Awadallah, M.; Idle, M.; Patel, K.; Kademani, D. Management update of potentially premalignant oral epithelial lesions. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2018, 125, 628–636.
Warnakulasuriya, S.; Johnson, N.W.; Van Der Waal, I. Nomenclature and classification of potentially malignant disorders of the oral mucosa. J. Oral Pathol. Med. 2007, 36, 575–580.
van der Waal, I. Potentially malignant disorders of the oral and oropharyngeal mucosa; present concepts of management. Oral Oncol. 2010, 46, 423–425.
Pentenero, M.; Meleti, M.; Vescovi, P.; Gandolfo, S. Oral proliferative verrucous leucoplakia: Are there particular features for such an ambiguous entity? A systematic review. Br. J. Dermatol. 2014, 170, 1039–1047.
Lombardi, N.; D’amore, F.; Elli, C.; Pispero, A.; Moneghini, L.; Franchini, R. Gingival lesion in proliferative verrucous leukoplakia. Dent. Cadmos 2020, 88, 647–648, doi:10.19256/d.cadmos.10.2020.03.
Hansen, L.S.; Olson, J.A.; Silverman, S. Proliferative verrucous leukoplakia. A long-term study of thirty patients. Oral Surgery, Oral Med. Oral Pathol. 1985, doi:10.1016/0030-4220(85)90313-5.
Villa, A.; Menon, R.S.; Kerr, A.R.; De Abreu Alves, F.; Guollo, A.; Ojeda, D.; Woo, S.B. Proliferative leukoplakia: Proposed new clinical diagnostic criteria. Oral Dis. 2018, 24, 749–760,
Aguirre-Urizar, J.M. Proliferative multifocal leukoplakia better name that proliferative verrucous leukoplakia. World J. Surg. Oncol. 2011, 9.
Lombardi, N.; Varoni, E.M.; Moneghini, L.; Lodi, G. Submucosal oral squamous cell carcinoma of the tongue. Oral Oncol. 2020, 105121, doi:10.1016/j.oraloncology.2020.105121.
Lodi, G.; Tarozzi, M.; Baruzzi, E.; Costa, D.; Franchini, R.; D’Amore, F.; Carassi, A.; Lombardi, N. Odontoiatria e cancro della bocca: dai fattori di rischio alla riabilitazione – Modulo 1: Epidemiologia e fattori di rischio. Dent. Cadmos 2021, 89, 01, doi:10.19256/d.cadmos.01.2021.14.
Lombardi, N.; Sorrentino, D.; D’amore, F.; Moneghini, L.; Franchini, R.; Sardella, A. Oral erythroleukoplakia on the lateral border of the tongue in a young patient. Dent. Cadmos 2020, 88, 277–278, doi:10.19256/d.cadmos.05.2020.03.
Warnakulasuriya, S.; Ariyawardana, A. Malignant transformation of oral leukoplakia: A systematic review of observational studies. J. Oral Pathol. Med. 2016, 45, 155–166, doi:10.1111/jop.12339.
Ho, M.W.; Risk, J.M.; Woolgar, J.A.; Field, E.A.; Field, J.K.; Steele, J.C.; Rajlawat, B.P.; Triantafyllou, A.; Rogers, S.N.; Lowe, D.; et al. The clinical determinants of malignant transformation in oral epithelial dysplasia. Oral Oncol. 2012, 48, 969–976, doi:10.1016/j.oraloncology.2012.04.002.
Field, E.A.; McCarthy, C.E.; Ho, M.W.; Rajlawat, B.P.; Holt, D.; Rogers, S.N.; Triantafyllou, A.; Field, J.K.; Shaw, R.J. The management of oral epithelial dysplasia: The Liverpool algorithm. Oral Oncol. 2015, 51, 883–887.
van der Waal, I. Potentially malignant disorders of the oral and oropharyngeal mucosa; terminology, classification and present concepts of management. Oral Oncol. 2009.
Diz P, Gorsky M, Johnson NW, Kragelund C, Manfredi M, Odell E, et al. Oral leukoplakia and erythroplakia: a protocol for diagnosis and management. EAOM – Diagnostic Ther. Protoc. 2011, 1, 1-8.
Van der Waal, I.; Axéll, T. Oral leukoplakia: A proposal for uniform reporting. Oral Oncol. 2002, 38, 521–526.
Reddi, S.P.; Shafer, A.T. Oral Premalignant Lesions: Management Considerations. Oral Maxillofac. Surg. Clin. North Am. 2006, 18, 425–433.
Pereira, J.D.S.; Carvalho, M.D.V.; Henriques, Á.C.G.; De Queiroz Camara, T.H.; Miguel, M.C.D.C.; Freitas, R.D.A. Epidemiology and correlation of the clinicopathological features in oral epithelial dysplasia: Analysis of 173 cases. Ann. Diagn. Pathol. 2011, 15, 98–102, doi:10.1016/j.anndiagpath.2010.08.008.
Rock, L.D.; Rosin, M.P.; Zhang, L.; Chan, B.; Shariati, B.; Laronde, D.M. Characterization of epithelial oral dysplasia in non-smokers: First steps towards precision medicine. Oral Oncol. 2018, 78, 119–125, doi:10.1016/j.oraloncology.2018.01.028.
Dilhari, A.; Weerasekera, M.M.; Siriwardhana, A.; Maheshika, O.; Gunasekara, C.; Karunathilaka, S.; Nagahawatte, A.; Fernando, N. Candida infection in oral leukoplakia: an unperceived public health problem. Acta Odontol. Scand. 2016, 74, 565–569, doi:10.1080/00016357.2016.1220018.
Speight, P.M. Update on oral epithelial dysplasia and progression to cancer. Head Neck Pathol. 2007, 1, 61–66, doi:10.1007/s12105-007-0014-5.
Warnakulasuriya, S.; Kovacevic, T.; Madden, P.; Coupland, V.H.; Sperandio, M.; Odell, E.; Møller, H. Factors predicting malignant transformation in oral potentially malignant disorders among patients accrued over a 10-year period in South East England. J. Oral Pathol. Med. 2011, 40, 677–683, doi:10.1111/j.1600-0714.2011.01054.x.
Arduino, P.G.; Surace, A.; Carbone, M.; Elia, A.; Massolini, G.; Gandolfo, S.; Broccoletti, R. Outcome of oral dysplasia: A retrospective hospital-based study of 207 patients with a long follow-up. J. Oral Pathol. Med. 2009, 38, 540–544, doi:10.1111/j.1600-0714.2009.00782.x.
Watabe, Y.; Nomura, T.; Onda, T.; Yakushiji, T.; Yamamoto, N.; Ohata, H.; Takano, N.; Shibahara, T. Malignant transformation of oral leukoplakia with a focus on low-grade dysplasia. J. Oral Maxillofac. Surgery, Med. Pathol. 2016, 28, 26–29, doi:10.1016/j.ajoms.2015.02.007.
Kujan, O.; Oliver, R.J.; Khattab, A.; Roberts, S.A.; Thakker, N.; Sloan, P. Evaluation of a new binary system of grading oral epithelial dysplasia for prediction of malignant transformation. Oral Oncol. 2006, doi:10.1016/j.oraloncology.2005.12.014.
El-Naggar A.K., Chan J.K.C., Grandis J.R., Takata T., S.P.J. WHO classification of Head and Neck tumors; 4th ed.; IARC Press: Lyon, 2017; ISBN 9789283224372.
Thomson, P. Oral Precancer; Thomson, P., Ed.; John Wiley & Sons, Ltd.: West Sussex, UK, 2012; ISBN 9781118702840.
Warnakulasuriya, S.; Reibel, J.; Bouquot, J.; Dabelsteen, E. Oral epithelial dysplasia classification systems: Predictive value, utility, weaknesses and scope for improvement. J. Oral Pathol. Med. 2008, 37, 127–133.
Pentenero, M.; Carrozzo, M.; Pagano, M.; Galliano, D.; Broccoletti, R.; Scully, C.; Gandolfo, S. Oral mucosal dysplastic lesions and early squamous cell carcinomas: Underdiagnosis from incisional biopsy. Oral Dis. 2003, 9, 68–72, doi:10.1034/j.1601-0825.2003.02875.x.
Lee, J.J.; Hung, H.C.; Cheng, S.J.; Chen, Y.J.; Chiang, C.P.; Liu, B.Y.; Jeng, J.H.; Chang, H.H.; Kuo, Y.S.; Lan, W.H.; et al. Carcinoma and dysplasia in oral leukoplakias in Taiwan: Prevalence and risk factors. Oral Surgery, Oral Med. Oral Pathol. Oral Radiol. Endodontology 2006, 101, 472–480, doi:10.1016/j.tripleo.2005.07.024.
Cabay, R.J.; Morton, T.H.; Epstein, J.B. Proliferative verrucous leukoplakia and its progression to oral carcinoma: A review of the literature. J. Oral Pathol. Med. 2007, 36, 255–261, doi:10.1111/j.1600-0714.2007.00506.x.
Iocca, O.; Sollecito, T.P.; Alawi, F.; Weinstein, G.S.; Newman, J.G.; De Virgilio, A.; Di Maio, P.; Spriano, G.; Pardiñas López, S.; Shanti, R.M. Potentially malignant disorders of the oral cavity and oral dysplasia: A systematic review and meta-analysis of malignant transformation rate by subtype. Head Neck 2020, 42, 539–555.
Bagan, J.; Murillo-Cortes, J.; Poveda-Roda, R.; Leopoldo-Rodado, M.; Bagan, L. Second primary tumors in proliferative verrucous leukoplakia: a series of 33 cases. Clin. Oral Investig. 2020, 24, 1963–1969, doi:10.1007/s00784-019-03059-9.
Reibel, J.; Gale, N.; Hille, J.; Hunt, J.; Lingen, M.; Muller, S.; Sloan, P.; Tilakaratne, W.; Westra, W.; Williams, M.; et al. Oral potentially malignant disorders and oral epithelial dysplasia. In WHO classification of head and neck tumours; IARC, Ed.; Lyon France, 2017; pp. 112–115 ISBN 9789283224389.
Ranganathan, K.; Kavitha, L. Oral epithelial dysplasia: Classifications and clinical relevance in risk assessment of oral potentially malignant disorders. J. Oral Maxillofac. Pathol. 2019, 23, 19–27.
Barnes, L.; Eveson, J.W.; Reichart, P.; Sidransky, D. World Health Organization Classification of Tumours. Pathology & Genetics. Head and Neck Tumours. International Agency for Research on Cancer (IARC). WHO Classif. Tumours (3rd Ed. 2005, 177–80.
Lee, J.J.; Hung, H.C.; Cheng, S.J.; Chiang, C.P.; Liu, B.Y.; Yu, C.H.; Jeng, J.H.; Chang, H.H.; Kok, S.H. Factors associated with underdiagnosis from incisional biopsy of oral leukoplakic lesions. Oral Surgery, Oral Med. Oral Pathol. Oral Radiol. Endodontology 2007, 104, 217–225, doi:10.1016/j.tripleo.2007.02.012.
Meleti, M.; Giovannacci, I.; Vescovi, P.; Pedrazzi, G.; Govoni, P.; Magnoni, C. Histopathological determinants of autofluorescence patterns in oral carcinoma. Oral Dis. 2020, doi:10.1111/odi.13304.
Tiwari, L.; Kujan, O.; Farah, C.S. Optical fluorescence imaging in oral cancer and potentially malignant disorders: A systematic review. Oral Dis. 2020.
Warnakulasuriya, S. White, red, and mixed lesions of oral mucosa: A clinicopathologic approach to diagnosis. Periodontol. 2000 2019, 80, 89–104.
Auluck, A.; Pai, K.M. (Mis)interpretations of leukoplakia. J. Can. Dent. Assoc. (Tor). 2005.
Müller, S. Frictional Keratosis, Contact Keratosis and Smokeless Tobacco Keratosis: Features of Reactive White Lesions of the Oral Mucosa. Head Neck Pathol. 2019, 13, 16–24.
Kramer, I.R.; El, L.; Lee, K.W. The clinical features and risk of malignant transformation in sublingual keratosis. Br. Dent. J. 1978, 144, 171–180, doi:10.1038/sj.bdj.4804055.
Eversole, L.R.; Eversole, G.M.; Kopcik, J. Sanguinaria-associated oral leukoplakia: Comparison with other benign and dysplastic leukoplakic lesions. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. Endod. 2000, 89, 455–464, doi:10.1016/S1079-2104(00)70125-9.
Gupta, P.C.; Mehta, F.S.; Daftary, D.K. Incidence rates of oral cancer and natural history of oral precancerous lesions in a 10-year follow-up study of Indian villagers. Community Dent. Oral Epidemiol. 1980, 8, 287–333, doi:10.1111/j.1600-0528.1980.tb01302.x.
Sreenivasa Bharath, T.; Govind Raj Kumar, N.; Nagaraja, A.; Saraswathi, T.R.; Suresh Babu, G.; Ramanjaneya Raju, P. Palatal changes of reverse smokers in a rural coastal Andhra population with review of literature. J. Oral Maxillofac. Pathol. 2015, 19, 182–187, doi:10.4103/0973-029X.164530.
Woo, S. Bin; Grammer, R.L.; Lerman, M.A. Keratosis of unknown significance and leukoplakia: A preliminary study. Oral Surg. Oral Med. Oral Pathol. Oral Radiol. 2014, 118, 713–724, doi:10.1016/j.oooo.2014.09.016.
Villa, A.; Hanna, G.J.; Kacew, A.; Frustino, J.; Hammerman, P.S.; Woo, S. Bin Oral keratosis of unknown significance shares genomic overlap with oral dysplasia. Oral Dis. 2019, 25, 1707–1714, doi:10.1111/odi.13155.
Lodi, G.; Porter, S. Management of potentially malignant disorders: Evidence and critique. J. Oral Pathol. Med. 2008, 37, 63–69.
Kanatas, A.N.; Fisher, S.E.; Lowe, D.; Ong, T.K.; Mitchell, D.A.; Rogers, S.N. The configuration of clinics and the use of biopsy and photography in oral premalignancy: A survey of consultants of the British Association of Oral and Maxillofacial Surgeons. Br. J. Oral Maxillofac. Surg. 2011, 49, 99–105, doi:10.1016/j.bjoms.2010.01.016.
Kumar, A.; Cascarini, L.; McCaul, J.A.; Kerawala, C.J.; Coombes, D.; Godden, D.; Brennan, P.A. How should we manage oral leukoplakia? Br. J. Oral Maxillofac. Surg. 2013, 51, 377–383, doi:10.1016/j.bjoms.2012.10.018.
Dionne, K.R.; Warnakulasuriya, S.; Zain, R.B.; Cheong, S.C. Potentially malignant disorders of the oral cavity: Current practice and future directions in the clinic and laboratory. Int. J. Cancer 2015, 136, 503–515.
Diajil, A.; Robinson, C.M.; Sloan, P.; Thomson, P.J. Clinical Outcome Following Oral Potentially Malignant Disorder Treatment: A 100 Patient Cohort Study. Int. J. Dent. 2013, 2013, 1–8, doi:10.1155/2013/809248.
Ribeiro, A.S.; Salles, P.R.; da Silva, T.A.; Mesquita, R.A. A Review of the Nonsurgical Treatment of Oral Leukoplakia. Int. J. Dent. 2010, 2010, 1–10, doi:10.1155/2010/186018.
Jaiswal, G.; Jaiswal, S.; Kumar, R.; Sharma, A. Field cancerization: concept and clinical implications in head and neck squamous cell carcinoma. J. Exp. Ther. Oncol. 2013.
Arduino, P.G.; Lodi, G.; Cabras, M.; Macciotta, A.; Gambino, A.; Conrotto, D.; Karimi, D.; El Haddad, G.; Carbone, M.; Broccoletti, R. A Randomized Controlled Trial on Efficacy of Surgical Excision of non-dysplastic Leukoplakia to Prevent Oral Cancer. Cancer Prev. Res. 2020, canprevres.0234.2020, doi:10.1158/1940-6207.capr-20-0234.
Mehanna, H.M.; Rattay, T.; Smith, J.; McConkey, C.C. Treatment and follow-up of oral dysplasia – A systematic review and meta-analysis. Head Neck 2009, doi:10.1002/hed.21131.
Saito, T.; Sugiura, C.; Hirai, A.; Notani, K.I.; Totsuka, Y.; Shindoh, M.; Fukuda, H. Development of squamous cell carcinoma from pre-existent oral leukoplakia: With respect to treatment modality. Int. J. Oral Maxillofac. Surg. 2001, 30, 49–53.
Zhang, L.; Lubpairee, T.; Laronde, D.M.; Rosin, M.P. Should severe epithelial dysplasia be treated? Oral Oncol. 2016, 60, 125–129, doi:10.1016/j.oraloncology.2016.07.007.
Balasundaram, I.; Payne, K.F.B.; Al-Hadad, I.; Alibhai, M.; Thomas, S.; Bhandari, R. Is there any benefit in surgery for potentially malignant disorders of the oral cavity? J. Oral Pathol. Med. 2014.
Thomson, P.J.; McCaul, J.A.; Ridout, F.; Hutchison, I.L. To treat…or not to treat? Clinicians’ views on the management of oral potentially malignant disorders. Br. J. Oral Maxillofac. Surg. 2015, 53, 1027–1031, doi:10.1016/j.bjoms.2015.08.263.
Kuribayashi, Y.; Tsushima, F.; Morita, K.; Matsumoto, K.; Sakurai, J.; Uesugi, A.; Sato, K.; Oda, S.; Sakamoto, K.; Harada, H. Long-term outcome of non-surgical treatment in patients with oral leukoplakia. Oral Oncol. 2015, 51, 1020–1025, doi:10.1016/j.oraloncology.2015.09.004.
Mogedas-Vegara, A.; Hueto-Madrid, J.A.; Chimenos-Küstner, E.; Bescós-Atín, C. Oral leukoplakia treatment with the carbon dioxide laser: A systematic review of the literature. J. Cranio-Maxillofacial Surg. 2016, doi:10.1016/j.jcms.2016.01.026.







